题目内容
 2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )
2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )| A、0.01mol?L-1的醋酸溶液的pH=2 |
| B、向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数Ka会增大 |
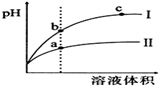
| C、等pH的盐酸与醋酸稀释后pH的变化如下图所示,则曲线I表示的是盐酸 |
| D、上图中,a、b、c三点表示的溶液的导电性强弱关系为b>a>c |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、醋酸是弱酸,不能完全电离;
B、电离常数Ka只受温度影响;
C、醋酸加水稀释时,氢离子物质的量增大,盐酸加水稀释时,氢离子物质的量不变;
D、离子浓度越大,溶液导电能力越强.
B、电离常数Ka只受温度影响;
C、醋酸加水稀释时,氢离子物质的量增大,盐酸加水稀释时,氢离子物质的量不变;
D、离子浓度越大,溶液导电能力越强.
解答:
解:A、0.01mol?L-1的醋酸溶液的pH>2,故A错误;
B、向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数Ka不变,故B错误;
C、醋酸加水稀释时,氢离子物质的量增大,盐酸加水稀释时,氢离子物质的量不变,所以盐酸pH变化大,故C正确;
D、上图中,a、b、c三点表示的溶液的导电性强弱关系为a>b>c,故D错误;
故选C.
B、向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数Ka不变,故B错误;
C、醋酸加水稀释时,氢离子物质的量增大,盐酸加水稀释时,氢离子物质的量不变,所以盐酸pH变化大,故C正确;
D、上图中,a、b、c三点表示的溶液的导电性强弱关系为a>b>c,故D错误;
故选C.
点评:本题考查了弱电解质存在电离平衡,加水稀释时强酸与弱酸离子浓度的变化、电离平衡常数指受温度影响、以及溶液导电性与离子浓度的关系.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
下列说法中,正确的是( )
| A、难溶电解质都是弱电解质 |
| B、难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止 |
| C、在白色ZnS沉淀上滴加CuSO4溶液,沉淀变黑色,说明CuS比ZnS更难溶于水 |
| D、相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同 |
对于苯乙烯的下列叙述其中完全正确的是( )
①能使酸性KMnO4溶液褪色;
②可发生加聚反应;
③可溶于水;
④可溶于苯中;
⑤苯环能与溴水发生取代反应;
⑥所有的原子可能共面,且最多有5个原子共线.
①能使酸性KMnO4溶液褪色;
②可发生加聚反应;
③可溶于水;
④可溶于苯中;
⑤苯环能与溴水发生取代反应;
⑥所有的原子可能共面,且最多有5个原子共线.
| A、①②④ | B、①②④⑥ |
| C、①②④⑤⑥ | D、①②③④⑤⑥ |
为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了下列四种不同的方法,其中不可行的是( )
| A、分别加入1 mol/L的盐酸溶液,看有无气泡产生 |
| B、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
| C、分别取样配成溶液,滴加BaCl2溶液,观察有无白色沉淀 |
| D、用焰色反应的方法区别 |
有关水在人体中的作用,下列说法正确的是( )
| A、自来水是很好的饮用水 |
| B、水在人体内还有调节体温的作用 |
| C、饮用水越纯净越好 |
| D、没有污染的水就是纯净水 |
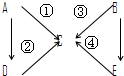 如图表示A-E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色.
如图表示A-E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色.(1)写出下列物质的化学式:A
(2)各步反应的化学方程式:
①
将0.2mol?L-1MOH溶液和0.1mol?L-1HCl的溶液等体积混合后,溶液呈酸性,下列关系式中不正确的是( )
| A、c(MOH)>c(M+) |
| B、c(M+)+c(H+)=c(Cl-)+c(OH-) |
| C、c(MOH)+c(M+)=0.2mol?L-1 |
| D、c(M+)<c(Cl-) |
下列关于钠及其化合物性质的叙述,正确的是( )
| A、钠能与硫酸铜稀溶液反应,置换出红色的铜 |
| B、氧化钠和过氧化钠都能与水反应,生成物完全相同 |
| C、过氧化钠是淡黄色固体,可用作呼吸面具的氧气来源 |
| D、热稳定性:Na2CO3<NaHCO3 |