题目内容
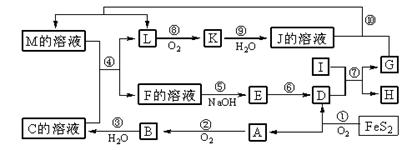
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出).其中,I是第三周期半径最小的金属元素组成的单质,K是一种红棕色气体.

请填写下列空白:
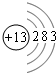
(1)A的化学式为______,I的原子结构示意图为______.
(2)在周期表中,组成单质G的元素在周期表中的位置是______.
(3)写出反应⑦的化学方程式______当有0.3mol电子转移时,生成G的物质的量为______.
(4)在反应②、③、⑥、⑨中,既属于化合反应又能属于非氧化还原反应的是______(填写序号).
(5)反应④的离子方程式是:______.
(6)将化合物D与KNO3、KOH混合,在高温条件下可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:______.
解:FeS2氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,I是第三周期半径最小的金属元素组成的单质,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,即铝热反应.K是一种红棕色气体,为NO2,则J为HNO3,L被氧化成为NO2,故L可能为氨或NO2,由于C溶液,即硫酸溶液能与某M溶液反应得到L,故L不可能是碱性的气体氨气,故L为NO,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,由反应4FeS2+11O2  2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,
2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,
(1)由以上分析可知A为SO2,I为Al,原子核外电子数为13,结构示意图为 ,故答案为:SO2;
,故答案为:SO2; ;
;
(2)由以上分析可知G为Fe,是26号元素,位于周期表第四周期第Ⅷ族,故答案为:第四周期第Ⅷ族;
(3)反应⑦为Al与Fe2O3所发生的置换反应,方程式为2Al+Fe2O3 2Fe+Al2O3,反应中铁元素化合价由+3价降低为0价,0.3mol电子转移时,生成Fe的物质的量为
2Fe+Al2O3,反应中铁元素化合价由+3价降低为0价,0.3mol电子转移时,生成Fe的物质的量为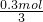 =0.1mol,故答案为:2Al+Fe2O3
=0.1mol,故答案为:2Al+Fe2O3 2Fe+Al2O3;0.1mol;
2Fe+Al2O3;0.1mol;
(4)在反应②、③、⑥、⑨中,②、⑥、⑨都为氧化还原反应,③为SO3+H2O=H2SO4的反应,既属于化合反应又属于非氧化还原反应,故答案为:③;
(5)M中含有Fe2+和NO3-,在酸性条件下可发生氧化还原反应,反应的离子方程式为Fe2++4H++NO3-=3Fe3++NO↑+2H2O,
故答案为:Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(6)化合物Fe2O3与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4,同时还生成KNO2和H2O,反应方程式为Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O,
2K2FeO4+3KNO2+2H2O,
故答案为:Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O.
2K2FeO4+3KNO2+2H2O.
分析:FeS2氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,I是第三周期半径最小的金属元素组成的单质,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,即铝热反应.K是一种红棕色气体,为NO2,则J为HNO3,L被氧化成为NO2,故L可能为氨或NO2,由于C溶液,即硫酸溶液能与某M溶液反应得到L,故L不可能是碱性的气体氨气,故L为NO,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,由反应4FeS2+11O2 2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,结合对应物质的性质和题目要求解答该题.
2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,结合对应物质的性质和题目要求解答该题.
点评:本题考查无机物的推断,题目难度中等,注意根据FeS2与氧气反应,结合反应特点和I是第三周期半径最小的金属元素组成的单质,K红棕色气体,先确定个别物质,根据框图寻找线索进行推断.
 2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,
2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,(1)由以上分析可知A为SO2,I为Al,原子核外电子数为13,结构示意图为
 ,故答案为:SO2;
,故答案为:SO2; ;
;(2)由以上分析可知G为Fe,是26号元素,位于周期表第四周期第Ⅷ族,故答案为:第四周期第Ⅷ族;
(3)反应⑦为Al与Fe2O3所发生的置换反应,方程式为2Al+Fe2O3
 2Fe+Al2O3,反应中铁元素化合价由+3价降低为0价,0.3mol电子转移时,生成Fe的物质的量为
2Fe+Al2O3,反应中铁元素化合价由+3价降低为0价,0.3mol电子转移时,生成Fe的物质的量为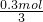 =0.1mol,故答案为:2Al+Fe2O3
=0.1mol,故答案为:2Al+Fe2O3 2Fe+Al2O3;0.1mol;
2Fe+Al2O3;0.1mol;(4)在反应②、③、⑥、⑨中,②、⑥、⑨都为氧化还原反应,③为SO3+H2O=H2SO4的反应,既属于化合反应又属于非氧化还原反应,故答案为:③;
(5)M中含有Fe2+和NO3-,在酸性条件下可发生氧化还原反应,反应的离子方程式为Fe2++4H++NO3-=3Fe3++NO↑+2H2O,
故答案为:Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(6)化合物Fe2O3与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4,同时还生成KNO2和H2O,反应方程式为Fe2O3+3KNO3+4KOH
 2K2FeO4+3KNO2+2H2O,
2K2FeO4+3KNO2+2H2O,故答案为:Fe2O3+3KNO3+4KOH
 2K2FeO4+3KNO2+2H2O.
2K2FeO4+3KNO2+2H2O.分析:FeS2氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,I是第三周期半径最小的金属元素组成的单质,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,即铝热反应.K是一种红棕色气体,为NO2,则J为HNO3,L被氧化成为NO2,故L可能为氨或NO2,由于C溶液,即硫酸溶液能与某M溶液反应得到L,故L不可能是碱性的气体氨气,故L为NO,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,由反应4FeS2+11O2
 2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,结合对应物质的性质和题目要求解答该题.
2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,结合对应物质的性质和题目要求解答该题.点评:本题考查无机物的推断,题目难度中等,注意根据FeS2与氧气反应,结合反应特点和I是第三周期半径最小的金属元素组成的单质,K红棕色气体,先确定个别物质,根据框图寻找线索进行推断.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目