题目内容
2.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )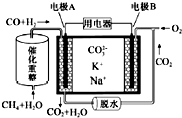
| A. | 电极B为正极,CO2在正极发生还原反应 | |
| B. | 电极A上H2参与的电极反应为:H2+CO32--2e-=CO2↑+H2O | |
| C. | 电极B上发生的电极反应为:4H++O2+4e-=2H2O | |
| D. | 电池工作时,CO32-向电极B移动 |
分析 甲烷和水经催化重整生成CO和H2,原电池工作时,CO和H2为负极反应,被氧化生成二氧化碳和水,正极为氧气得电子生成CO32-,以此解答该题.
解答 解:A.CO和H2为负极反应,被氧化生成二氧化碳和水,正极为氧气得电子生成CO32-,故A错误;
B.CO和H2为负极反应,被氧化生成二氧化碳和水,电极A上H2参与的电极反应为:H2+CO+2CO32--4e-=H2O+3CO2,故B正确;
C.B为正极,正极为氧气得电子生成CO32-,反应为O2+2CO2+4e-=2CO32-,故C错误;
D.电池工作时,CO32-向负极移动,即向电极A移动故D错误.
故选B.
点评 本题考查了化学电源新型电池,明确原电池中物质得失电子、电子流向、离子流向即可解答,难点是电极反应式书写,要根据电解质确定正负极产物,难度中等.

练习册系列答案
相关题目
12.有机物: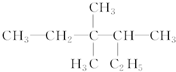 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 3,3二甲基4乙基戊烷 | B. | 3,3,4三甲基己烷 | ||
| C. | 2乙基3,3二甲基4乙基戊烷 | D. | 3,4,4三甲基己烷 |
13.维生素A的结构简式如图,下列关于它的说法正确的是( )
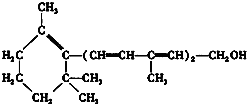

| A. | 维生素A是一种酚 | |
| B. | 维生素A的一个分子中有三个双键 | |
| C. | 维生素A可以使酸性高锰酸钾溶液褪色 | |
| D. | 维生素A具有环己烷的结构单元 |
10.两种元素可以组成AB2型化合物,它们的原子序数可能为( )
| A. | 6和8 | B. | 8和13 | C. | 10和14 | D. | 7和12 |
17.下列说法正确的是( )
| A. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | 第三周期元素的离子半径从左到右逐渐减小 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | ⅣA族元素的氢化物中,稳定性最好的是CH4 |
7.直接由原子构成的一组物质是( )
| A. | 干冰、二氧化硅、金刚石 | B. | 氧化钠、金刚石、氯化氢 | ||
| C. | 碘、石墨、氯化钠 | D. | 二氧化硅、金刚石、晶体硅 |
14.某有机物含有C、H、O、N等元素,该有机物可能是( )
| A. | 油脂 | B. | 葡萄糖 | C. | 蛋白质 | D. | 淀粉 |