题目内容
17.下列属于固氮作用的化学反应是( )| A. | N2和H2在一定条件下反应生成NH3 | B. | NO与O2反应生成NO2 | ||
| C. | NH3催化氧化生成NO和H2O | D. | 由NH3制NH4HCO3和(NH4)2SO4 |
分析 氮的固定是氮游离态的转化为化合态的过程,由单质转化为化合物都叫固氮,包括自然固氮和人工固氮.
解答 解:A.N2与H2在一定条件下反应生成NH3,氮由单质转化为化合物,属于氮的固定,故A正确;
B.NO遇O2转化为NO2,是氮元素不同化合物之间的转化,不属于氮的固定,故B错误;
C.硝酸工厂用NH3氧化制取NO,是氮元素不同化合物之间的转化,不属于氮的固定,故C错误;
D.由NH3制取碳酸铵,是氮元素不同化合物之间的转化,不属于氮的固定,故D错误;
故选A.
点评 本题考查了氮的固定的概念,判断氮的固定的关键是抓住氮元素的化合价是否从0价变为其他化合价,即从单质转化为化合物.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
7.下列物质中均既有离子键又有共价键的一组是( )
| A. | NaOH、H2O、NH4Cl | B. | KOH、Na2O2、NH4Cl | ||
| C. | MgO、CaBr2、NaCl | D. | Na2SO4、HCl、MgCl2 |
8.下列物质的电子式书写正确的是( )
| A. | 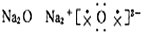 | B. | 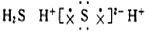 | C. | 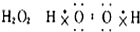 | D. | N2 N:::N |
5.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下表所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 四种元素的单质中,Z单质的熔沸点最高 | |
| D. | X的单质能与H2反应,生成一种弱酸性的物质 |
12.下列分子中所有碳原子不可能处在同一平面上的是( )
| A. |  | B. | 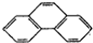 | C. |  | D. |  |
2.下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是②(填编号);
(2)元素⑨和⑩形成的化合物的化学式为Si3N4;元素⑦的原子价电子排布式是3s23p5;
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是π键(填σ或π),在高中化学中有一种常见分子的结合方式与O3相同,它是SO2(填分子式);
(4)根据对角线规则,Be与元素④的最高价氧化物的水化物的性质相似,它们都具有两性,显示这种性质的离子方程式是Be(OH)2+2H+═Be2++2H2O、Be(OH)2+2OH-═BeO22-+2H2O;
(5)由以上某些元素形成的有机物苯酚(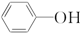 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子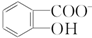 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是 中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
| 元素 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中,第一电离能最小的是②(填编号);
(2)元素⑨和⑩形成的化合物的化学式为Si3N4;元素⑦的原子价电子排布式是3s23p5;
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是π键(填σ或π),在高中化学中有一种常见分子的结合方式与O3相同,它是SO2(填分子式);
(4)根据对角线规则,Be与元素④的最高价氧化物的水化物的性质相似,它们都具有两性,显示这种性质的离子方程式是Be(OH)2+2H+═Be2++2H2O、Be(OH)2+2OH-═BeO22-+2H2O;
(5)由以上某些元素形成的有机物苯酚(
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是 中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
9.在1000mL含等物质的量的HI和H2SO3的溶液里通入0.25molCl2,有二分之一的HI变为I2(已知反应:I2+H2SO3+H2O=4H++SO42-+2I-).原溶液中HI和H2SO3的浓度都等于( )
| A. | 0.2 mol•L-1 | B. | 0.1 mol•L-1 | C. | 2.0 mol•L-1 | D. | 1.0 mol•L-1 |
7.下列化学用语正确的是( )
| A. | 乙烯结构简式为C2H4 | B. | 乙醇的比例模型为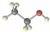 | ||
| C. | 间二甲苯的结构简式为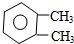 | D. | 甲烷的结构式为 |