题目内容
11.NA为阿伏加德罗常数,下列叙述正确的是( )| A. | 80g硝酸铵含有氮原子数为2NA | |
| B. | 1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 标准状况下,11.2L蒸馏水所含分子数为0.5NA | |
| D. | 在铜与硫的反应中,1mol铜失去的电子数为2NA |
分析 A、根据硝酸铵的质量计算出氮原子的物质的量及数目;
B.盐酸溶液中不存在HCl分子;
C.标准状况下蒸馏水不是气体,气体摩尔体积标准状况下为22.4L/mol;
D.铜与硫的反应生成硫化亚铜;
解答 解:A、80gNH4NO3的物质的量n=$\frac{m}{M}$=$\frac{80g}{80g/mol}$=1mol,氮原子个数=2n•NA=2NA,故A正确;
B.1L 1mol/L的盐酸溶液中,氯化氢完全电离不含氯化氢分子,故B错误;
C.标准状况下蒸馏水不是气体,11.2L蒸馏水物质的量不是0.5mol,故C错误;
D.铜与硫反应生成Cu2S,1mol铜失去的电子数为NA,故D错误;
故选A.
点评 本题考查阿伏加德罗常数,做题时注意物质的状态、存在的条件、物质的性质和分子的组成等因素,题目难度不大,本题注意硫和铜的反应物.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
18.关于Na2CO3和NaHCO3性质的说法正确的是( )
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 相同温度时的水溶性:Na2CO3<NaHCO3 | |
| C. | 等物质的量浓度的溶液的碱性:Na2CO3<NaHCO3 | |
| D. | 与同浓度的盐酸反应的剧烈程度:Na2CO3>NaHCO3 |
2.宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”涉及的化学反应是 4Ag+2H2S+O2═2X+2H2O,下列说法正确的是( )
| A. | X的化学式为AgS | B. | 每生成1mo1X转移2mo1电子 | ||
| C. | 反应的还原剂是H2S | D. | 银针验毒时,空气中氧气失去电子 |
19.在“固体干冰→液体二氧化碳→气体二氧化碳→气体一氧化碳”的变化过程中,被破坏的作用力依次是
( )
( )
| A. | 范德华力、范德华力、范德华力 | B. | 范德华力、范德华力、共价键 | ||
| C. | 范德华力、共价键、共价键 | D. | 共价键、共价键、共价键 |
20.25℃时,某溶液中由水电离出的c(OH-)=1×10-13mol/L,该溶液中一定不能大量共存的离子组是( )
| A. | SO42-、Na+、HCO3- | B. | CO32-、K+、Na+ | C. | Na+、SO42-、C1- | D. | NH4+、Fe3+、C1- |
1.下列有关胶体的说法不正确的是( )
| A. | 胶体带电荷,溶液不带电荷 | |
| B. | 胶体区别于其它分散系的本质特征是分散质的直径大小 | |
| C. | 将一柬光线通过胶体时可出现一条光亮的通路,通过溶液则没有此现象 | |
| D. | 土壤胶粒的表面巨大且带负电,能吸附NH${\;}_{4}^{+}$等营养离子,使土壤具有保肥能力 |
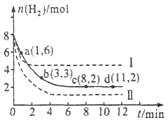 工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. $→_{△}^{浓H_{2}SO_{4}}$CH3CH=C(CH3)COOH+H2O.
$→_{△}^{浓H_{2}SO_{4}}$CH3CH=C(CH3)COOH+H2O.