题目内容
12.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )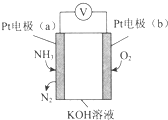
| A. | 溶液中OH-向电极a移动 | |
| B. | O2在电极b上发生还原反应 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | 电极a的反应式为2NH3-6e-+6OH-═N2+6H2O |
分析 Pt电子通入氨气生成氮气,说明氨气被氧化,为原电池负极,则b为正极,氧气得电子被还原,结合电极方程式解答该题.
解答 解:A.因为a极为负极,则溶液中的阴离子向负极移动,故A正确;
B.氧气在b极发生还原反应,则b极为正极,a极为负极,故B正确;
C.反应中N元素化合价升高3价,O元素化合价降低4价,根据得失电子守恒,消耗NH3与O2的物质的量之比为4:3,故C错误;
D.负极是氨气发生氧化反应变成氮气,且OH-向a极移动参与反应,故电极反应式为2NH3-6e-+6OH-=N2+6H2O,故D正确.
故选C.
点评 本题考查了原电池原理,根据O、N元素化合价变化判断正负极,再结合反应物、生成物及得失电子书写电极反应式,注意书写电极反应式时要结合电解质特点,为易错点.

练习册系列答案
相关题目
13.分类方法在化学学科的发展中起到了非常重要的作用,下列分类方法标准合理的是( )
(1)分子中含有的氢原子个数将酸分子分为一元酸、二元酸等
(2)根据反应是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
(3)根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
(4)根据反应中的热效应将化学反应分为放热反应和吸热反应
(5)根据氧化物的组成将所有的氧化物分为碱性、两性和酸性氧化物
(6)微粒间相互作用可分为化学键(如离子键、共价键、氢键等)和分子间作用力.
(1)分子中含有的氢原子个数将酸分子分为一元酸、二元酸等
(2)根据反应是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
(3)根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
(4)根据反应中的热效应将化学反应分为放热反应和吸热反应
(5)根据氧化物的组成将所有的氧化物分为碱性、两性和酸性氧化物
(6)微粒间相互作用可分为化学键(如离子键、共价键、氢键等)和分子间作用力.
| A. | (1)(3) | B. | (2)(4) | C. | (1)(2)(4)(6) | D. | (2)(3)(4)(5) |
3.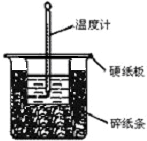 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌器.
(2)烧杯间填满碎纸条的作用是减少实验过程中的热量损失.
(3)要重复进行三次实验的目的是减少实验误差.
(4)大烧杯上如不盖硬纸板,求得的中和热数值偏小(填“偏大、偏小、无影响”);当室温低于10℃时进行,对实验结果会造成较大的误差,其原因是体系内、外温差大,会造成热量损失.
(5)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等、不相等”),所求中和热相等(填“相等、不相等”),简述理由因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关.
(6)用相同浓度和体积的醋酸(CH3COOH)代替HCl溶液进行上述实验,测得的中和热的数值会偏小;(填“偏大、偏小、无影响”).
(7)三次平行操作所测得的数据如下:
若上述HCl、NaOH溶液的密度都近似为1g/cm3,中和后生成的溶液的比热容C=4.18J/(g•℃),则实验测得的中和热为-39.3kJ/mol.
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌器.
(2)烧杯间填满碎纸条的作用是减少实验过程中的热量损失.
(3)要重复进行三次实验的目的是减少实验误差.
(4)大烧杯上如不盖硬纸板,求得的中和热数值偏小(填“偏大、偏小、无影响”);当室温低于10℃时进行,对实验结果会造成较大的误差,其原因是体系内、外温差大,会造成热量损失.
(5)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等、不相等”),所求中和热相等(填“相等、不相等”),简述理由因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关.
(6)用相同浓度和体积的醋酸(CH3COOH)代替HCl溶液进行上述实验,测得的中和热的数值会偏小;(填“偏大、偏小、无影响”).
(7)三次平行操作所测得的数据如下:
| 温度 序号 | 起始温度t1/℃ | 终止温度 T2/℃ | 温度差 △t/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25 | 25 | 27.3 | ||
| 2 | 25 | 25 | 27.4 | ||
| 3 | 25 | 25 | 28.6 | ||
20.下列物质不能使酸性高锰酸钾溶液褪色的是( )
| A. | 乙烯 | B. | 乙醇 | C. | 苯 | D. | 二氧化硫 |
7.一定条件下,容积为1L的密闭容器中发生反应:
SiF4(g)+2H2O(g)?SiO2(s)+4HF(g)△H=+148.9kJ•mol-1
下列各项中不能说明该反应已达化学平衡状态的是( )
SiF4(g)+2H2O(g)?SiO2(s)+4HF(g)△H=+148.9kJ•mol-1
下列各项中不能说明该反应已达化学平衡状态的是( )
| A. | v(SiF4)消耗=4v(HF)生成 | B. | HF的体积分数不再变化 | ||
| C. | 容器内气体压强不再变化 | D. | 容器内气体的总质量不再变化 |
2.下列说法正确的是( )
| A. | 金属钠着火可用水扑灭 | |
| B. | 将几滴FeCl3饱和溶液滴入氢氧化钠溶液可制备Fe(OH)3胶体 | |
| C. | 向含有等量NaI、NaCl的溶液中逐滴加入AgNO3溶液,先产生浅黄色沉淀 | |
| D. | 用浓氢氧化钠溶液和湿润红色石蕊试纸检验某溶液中是否有NH4+ |
 .
.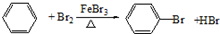 ,反应类型:取代反应.
,反应类型:取代反应.