题目内容
下列化合物中,含有非极性键的离子化合物是( )
| A、Ba(OH)2 |
| B、H2SO4 |
| C、Na2O2 |
| D、CaCl2 |
考点:离子化合物的结构特征与性质,极性键和非极性键
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,如第IA族、第IIA族元素和第VIA族、第VIIA族元素之间易形成离子键,不同非金属元素之间易形成极性共价键,同种非金属元素之间易形成非极性共价键,含有离子键的化合物是离子化合物.
解答:
解:A,氢氧化钡中钡离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,为含有极性键的离子化合物,故A错误;
B.硫酸中只含极性共价键,为共价化合物,故B错误;
C.过氧化钠中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在非极性键,为含有非极性键的离子化合物,故C正确;
D.氯化钙中钙离子和氯离子之间只存在离子键,为离子化合物,故D错误;
故选C.
B.硫酸中只含极性共价键,为共价化合物,故B错误;
C.过氧化钠中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在非极性键,为含有非极性键的离子化合物,故C正确;
D.氯化钙中钙离子和氯离子之间只存在离子键,为离子化合物,故D错误;
故选C.
点评:本题考查了化学键和化合物,根据物质的构成微粒及基本概念来分析解答,注意离子化合物不能根据是否含有金属元素判断,为易错点.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
下列各组物质中互称为同分异构体的是( )
| A、红磷与白磷 |
| B、水与重水 |
| C、乙醇(CH3CH2OH)与二甲醚(CH3OCH3) |
| D、O2与O3 |
下列分子中属于含极性键的非极性分子的是( )
| A、H2S |
| B、CH4 |
| C、Cl2 |
| D、NH3 |
下列反应中,不是氧化还原反应的是( )
A、H2+Cl2
| ||||
| B、Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||||
C、2H2O
| ||||
| D、CuO+2HNO3═Cu(NO3)2+H2O |
根据元素周期表和元素周期律,下列推断中错误的是( )
| A、砹是一种有色固体,它的气态氢化物很不稳定 |
| B、F2与水反应比Cl2与水反应剧烈 |
| C、铷的硫酸盐易溶解于水,其氢氧化物一定是弱碱 |
| D、氯化氢比溴化氢稳定,HClO4酸性强于HBrO4 |
下列物质的组成中一定含有氧元素的是( )
①水 ②酸 ③碱 ④盐 ⑤氧化物.
①水 ②酸 ③碱 ④盐 ⑤氧化物.
| A、只有① | B、只有①⑤ |
| C、①③⑤ | D、①②③④⑤ |
在无色透明的溶液中可以大量共存的离子组是( )
| A、OH-、K+、Al3+ |
| B、OH-、Cl-、NH4+ |
| C、Cu2+、NO3-、Cl- |
| D、Mg2+、K+、Cl- |
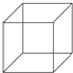 (1)键线式
(1)键线式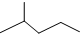 表示的分子式
表示的分子式