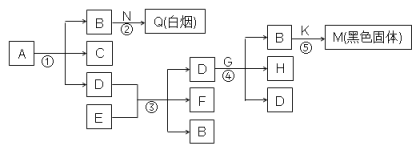
【题目】硫酸铜溶液能对过氧化氢的分解起催化作用.某小组拟在相同浓度硫酸铜溶液的催化下,探究硫酸铜对不同浓度过氧化氢溶液分解速率的影响.
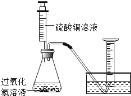
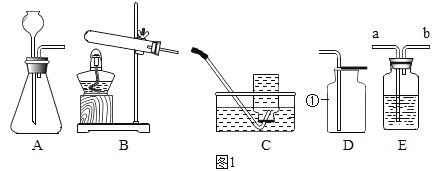
(1)分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的硫酸铜溶液,如图观察到产生气泡的速率不同,就可以粗略判断,得出实验结果.写出有关反应的化学方程式_____ ;
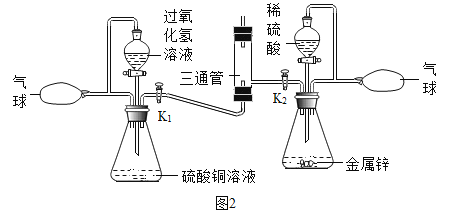
(2)为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设计.
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
[方案二]在不同过氧化氢浓度下,测定 ____________.
方案二的实验测量结果:
实验序号 物理量 | 过氧化氢溶液的浓度和体积 | 6%硫酸铜溶液的 体积(mL) | 反应的时间 (min) | 生成氧气的 体积(mL) |
1 | 8%10mL | x | 5 | V1 |
2 | 16%10mL | 3 | 5 | V2 |
表中x= _____.
实验结论:通过测量,若V1<V2,说明其它条件相同时, _________.
[继续探究]除了上述探究的影响反应速率的因素外,还有哪些因素可能会影响过氧化氢分解的反应速率?_______________(答一条即可)
【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势如图2所示。
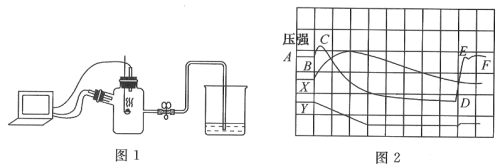
(1)红磷燃烧的化学反应符号表达式为________________________;
(2)X曲线表示的是____________(填“温度”或“氧气的浓度”);
(3)结合X、Y两条曲线,解释图2中BC段气压变化的原因是_________________________;
(4)实验中测得的数据如下:
测量 项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 瓶中剩余气体的体积 | |
体积/mL | 80.0 | 46.4 | 126.0 |
根据实验数据计算:测得的空气中氧气的体积分数为________________(列出计算式即可)。
【题目】课堂上,老师和同学们探究了二氧化碳的性质。请回答问题。
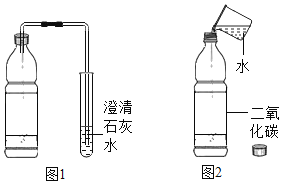
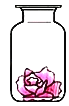
(学习情景)打开汽水瓶盖时,有气泡冒出。同学们将气体通入澄清石灰水中,石灰水变浑浊(如图),发生反应的化学方程式是_______________,实验后,老师要求同学们将试管中的浑浊物再次变得澄清,你认为可采用的方法是____________________。
(提出问题一)汽水中为什么会产生二氧化碳气体呢?
(作出猜想)汽水中溶有二氧化碳,二氧化碳能溶于水。
(进行实验)向一个收集满二氧化碳气体的质地较软的塑料瓶中加入![]() 体积的水、立即拧紧瓶盖,振荡,观察到的现象是_________________,得出二氧化碳能溶于水的洁论。
体积的水、立即拧紧瓶盖,振荡,观察到的现象是_________________,得出二氧化碳能溶于水的洁论。
(提出问题二)二氧化溶于水的过程中是否与水发生了化学反应?
(作出猜想)二氧化碳能与水发生化学反应,生成其它物质。
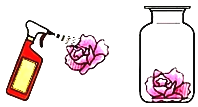
(实验方案)取三朵用紫色石蕊溶液染成紫色的干燥纸花,完成下列实验。
实验操作 | 实验现象及化学方程式 | 实验结论 |
步骤一:将第一朵纸花喷上稀醋酸 | 现象:紫色纸花变红 | 结论:二氧化碳能与水发生化学反应。化学方程式______________。 |
步骤二:将第二朵纸花直接放在盛滿二化碳的集气瓶中。 | 现象:紫色纸花没有变红 | |
步骤三:将第三朵纸花喷 上水后,再放入盛满二氧化碳的集气瓶中 | 现象: _________ | |
步骤四:将步骤三集气瓶 中的纸花取出,用吹风机烘干 | 现象: _________ | 结论: ________ |
(实验总结)汽水为混合物,至少含有以下三种物质:______。(用化学式表示)
【题目】课堂上、同学们对金属的性质展开如下探究,请你一起参与,并回答问题。
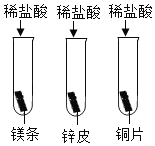
(1)甲小组进行了如图所示的实验,三支试管中分别放入用砂纸打磨过的镁条、锌皮和铜片,然后分别加入5mL稀盐酸,观察到的现象是______________________________,写出发生反应的一个化学方程式_________________________。
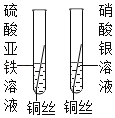
(2)乙小组设计实验、比较铁、铜、银的金属活动性强弱。
实验步骤(如图所示) | 实验现象 | 实验结论 |
| __________________ | 三种金属由强到弱的顺序是:铁>铜>银 |
请你再设计一种方案,得出与丙小组同学相同的结论,你选择的试剂是______。