【题目】今天又是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
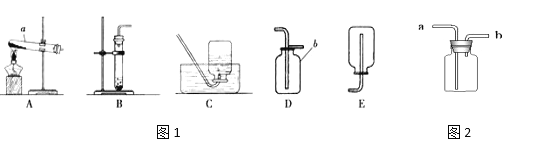
(1)写出图3中标有序号的仪器名称a_______
(2)①此气体是什么物质?验证它的实验方案如下:
猜想 | 实验步骤 | 现象及结论 |
此气体可能是:_____ | ______________ | ______________ |
②产生此气体的化学方程式可能是_________;
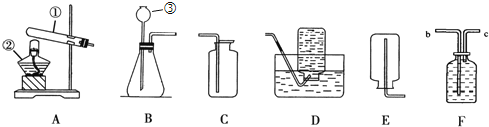
③我想制取该气体,可以分别选取图1中的______作发生装置和________作收集装置(填序号);
④如用图2装置收集该气体,气体由 ________端导入;
⑤若用加热高锰酸钾来制取氧气,所选用的发生装置是________(在图1中选择),产生氧气的化学方程式是:_____________。
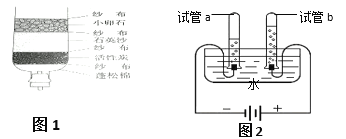
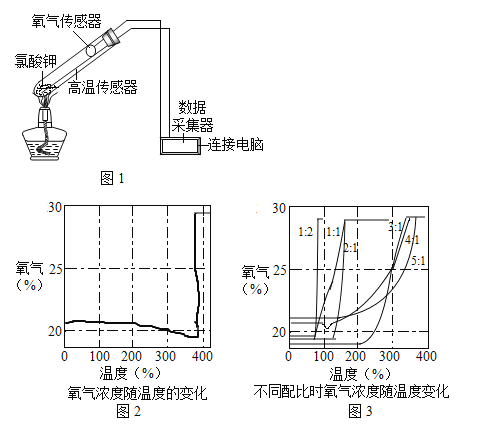
【题目】在老师的指导下,某学习小组利用如图1所示装置对氯酸钾(KClO3)制氧气进行了深入的探究学习。
资料:
①KClO3的熔点约为356℃,MnO2的分解温度约为535℃。用酒精灯物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指KClO3和MnO2混合物中,KClO3和MnO2的质量比;
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图及不同配比时氧气浓度随温度的变化示意图如图:
请回答问题:
(1)分析图2KClO3分解温度___(填“高于”、“等于”或“低于”)其熔点。
(2)分析图2在KClO3分解前,传感器得到氧气浓度降低的可能原因是___.
(3)分析图3KClO3分解温度随物质配比变化的规律是___,当物质配比为1:2是KClO3分解温度约为___℃。
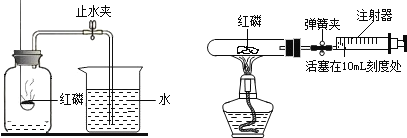
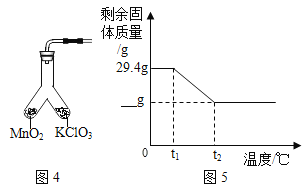
(4)为证实MnO2的催化作用,小组同学利用如图4装置进行如表所示的实验:
步骤 | 实验操作 | 实验现象 |
Ⅰ | 检查气密性 | |
Ⅱ | 分别在“Y”形管两侧支管中加入少量MnO2和KClO3,塞紧橡皮塞 | ________ |
Ⅲ | 分别先后加热MnO2和KClO3,用带火星木条放在导管口。加热___(填“左”或“右”)侧支管后,带火星木条复燃 | ________ |
Ⅳ | 冷却后,将“Y”形管左侧支管中部分MnO2混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口 | ________ |
请回答:
①完善步骤Ⅲ中的填空:
②步骤Ⅳ中,将MnO2混入右侧支管有余热的KClO3中的操作方法是___.
③步骤Ⅳ的实验现象能否说明MnO2是KClO3分解的催化剂___(填“能”或“不能”),如不能,还需证明在此反应中MnO2的___和___不变。
(5)将29.4gKClO3和MnO2混合物以5:1配比加热至完全反应,如图5中的值应为___。
A.4.9B.9.6C.14.9D.19.8.
【题目】合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献.合成氨工艺的主要流程如图1:

(1)合成塔中的反应必须在高温、高压、催化剂条件下进行,该反应化学方程式是:_______,属于_______(填基本反应类型)反应.
(2)生产过程中从合成塔中输出的气体属于_______(填“纯净物”或“混合物”).
(3)中生产过程中可重复使用的物质是________(填化学式).
(4)根据表中的数据回答问题.
物质 | H2 | N2 | O2 | NH3 |
沸点/℃(1.01×105Pa) | -252 | -195.8 | -183 | -33.35 |
在1.01×105Pa时,欲将NH3与N2、H2分离,最好将温度控制在_______之间.
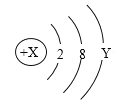
(5)图2是合成塔中发生反应的微观粒子示意图:由图可知两种反应物N2与H2的分子个数比为_______;
该反应中的最小粒子是_______(填写化学符号).