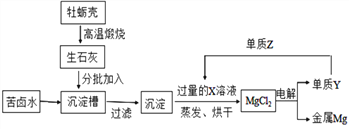
【题目】碳酸钠是苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸钠的性质,将一定质量的碳酸钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_________________________________________,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
【实验用品】pH试纸、锌片、氧化铜粉末,稀硫酸、氢氧化钠溶液、氯化钡溶液。
【猜想与假设】反应后溶液中溶质的可能组成成分
猜想一: ______________ 猜想二:硫酸钠、碳酸钠 猜想三:硫酸钠、硫酸
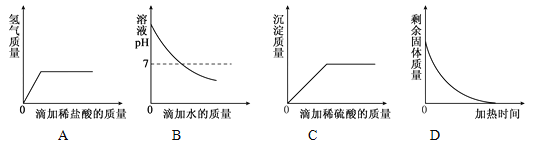
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表实验现象中的①②③。
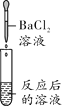
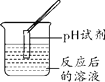
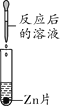
实验方案 | A | B | C | D |
实验操作 |
|
|
|
|
实验现象 | ______ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH____7 | ______ |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
【得出结论】猜想三正确。
【评价反思】(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显操作错误是:_______________________;
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由________________。
【总结提高】依据所给实验用品,设计不同的方案确认猜想三是正确的。请你写出你的实验方案_______________。