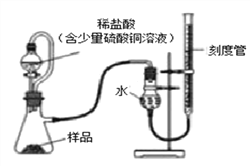
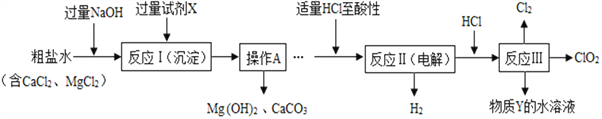
【题目】海洋中蕴藏着丰富的化学资源,如NaCl、MgCl2、CaCl2等物质。从海水中提取金属镁的主要流程如下:

(1)电解熔融的无水MgCl2可以得到金属镁。该反应属于基本反应类型中的 反应。
(2)将海水中的镁提取出来,首先要让海水中的镁离子形成沉淀而富集起来。结合表中数据分析,为了使氯化镁转化为沉淀,应加入溶液A可能是 。
室温下几种物质的溶解度
物质 | MgCO3 | CaCO3 | Mg(OH)2 | Ca(OH)2 |
溶解度/g | 0.01 | 0.0013 | 0.0029 | 0.16 |

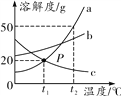
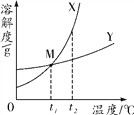
(3)结合MgCl2的溶解度曲线分析,操作I:蒸发浓缩、 、过滤。