5.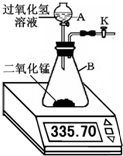 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
请根据要求回答下列问题:
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.
 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 装置+过氧化氢溶液 +二氧化锰/g | 335.70 | 335.68 | 335.54 | 335.18 | 334.46 | 334.10 | 334.10 |
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.
4.通过一段时间的化学学习,相信你已经掌握了实验室制取氧气的有关知识.请结合图示回答问题.

(1)写出图中标示的仪器名称:①酒精灯 ②集气瓶.
(2)实验室用氯酸钾和二氧化锰制取氧气:
写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,属于分解反应(填基本反应类型).若需要比较纯净的氧气用作铁丝燃烧实验,则收集装置最好选用F(填序号),运用以上收集装置的原因是做此实验时集气瓶底部要留少量水;防止溅落物炸裂瓶底.铁丝在氧气中燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;实验现象剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体.
(4)小珍阅读课外资料得知:用氯酸钾制取氧气时,除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【查阅资料】二氧化锰、氧化铜均为不溶于水的黑色粉末.
【设计实验】小珍以生成等体积的氧气为标准,设计了下列三组实验:
(其它可能影响实验的因素均忽略).
Ⅰ、上述实验应测量的“待测数据”是收集等量氧气所需时间.
Ⅱ、若实验②比实验①的“待测数据”更小(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
【质疑】这样能说明氧化铜是氯酸钾分解的催化剂吗?
【预期结论】不能.
【设计实验】将实验②反应后的固体加水充分溶解、过滤、洗涤、干燥、称量,此过程中需要用到的玻璃仪器有烧杯、漏斗、玻璃棒,第二步操作时耗时较长的原因可能是操作不规范.
若最终称量得到0.5g黑色粉末,应再将黑色粉末放入试管中,向试管中倒入适量的氯酸钾,混合均匀后加热,产生使带火星的木条复燃的气体(简述操作和现象).
【结论】氧化铜能作氯酸钾的催化剂.
【评价设计】你认为小珍设计实验③和实验②对比的目的是探究氧化铜和二氧化锰哪一个催化效果好.
(3)若用图I装置收集较为干燥的氧气,如何验满?将带火星的木条放在集气瓶口,如果复燃,说明收集满了.
(4)实验室用装置E制取氧气,如用注射器C替换长颈漏斗,优点是能够控制反应速率.
(5)注射器C也可用于检查装置E的气密性,步骤如下:
Ⅰ、向锥形瓶中加入少量水,使长颈漏斗插入液面以下.Ⅱ、将注射器C连接到装置E的导管口处.Ⅲ、缓慢拉动注射器C的活塞,观察到长颈漏斗下端形成一段水柱,表示装置E的气密性良好.

(1)写出图中标示的仪器名称:①酒精灯 ②集气瓶.
(2)实验室用氯酸钾和二氧化锰制取氧气:
写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,属于分解反应(填基本反应类型).若需要比较纯净的氧气用作铁丝燃烧实验,则收集装置最好选用F(填序号),运用以上收集装置的原因是做此实验时集气瓶底部要留少量水;防止溅落物炸裂瓶底.铁丝在氧气中燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;实验现象剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体.
(4)小珍阅读课外资料得知:用氯酸钾制取氧气时,除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【查阅资料】二氧化锰、氧化铜均为不溶于水的黑色粉末.
【设计实验】小珍以生成等体积的氧气为标准,设计了下列三组实验:
| 实验序号 | 氯酸钾质量 | 其它物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | 氧化铜0.5g | |
| ③ | 1.2g | 二氧化锰0.5g |
Ⅰ、上述实验应测量的“待测数据”是收集等量氧气所需时间.
Ⅱ、若实验②比实验①的“待测数据”更小(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
【质疑】这样能说明氧化铜是氯酸钾分解的催化剂吗?
【预期结论】不能.
【设计实验】将实验②反应后的固体加水充分溶解、过滤、洗涤、干燥、称量,此过程中需要用到的玻璃仪器有烧杯、漏斗、玻璃棒,第二步操作时耗时较长的原因可能是操作不规范.
若最终称量得到0.5g黑色粉末,应再将黑色粉末放入试管中,向试管中倒入适量的氯酸钾,混合均匀后加热,产生使带火星的木条复燃的气体(简述操作和现象).
【结论】氧化铜能作氯酸钾的催化剂.
【评价设计】你认为小珍设计实验③和实验②对比的目的是探究氧化铜和二氧化锰哪一个催化效果好.
(3)若用图I装置收集较为干燥的氧气,如何验满?将带火星的木条放在集气瓶口,如果复燃,说明收集满了.
(4)实验室用装置E制取氧气,如用注射器C替换长颈漏斗,优点是能够控制反应速率.
(5)注射器C也可用于检查装置E的气密性,步骤如下:
Ⅰ、向锥形瓶中加入少量水,使长颈漏斗插入液面以下.Ⅱ、将注射器C连接到装置E的导管口处.Ⅲ、缓慢拉动注射器C的活塞,观察到长颈漏斗下端形成一段水柱,表示装置E的气密性良好.
20.用表中的元素组成适当的物质(用化学式填空),回答下列问题:
(1)引起温室效应的主要物质是H2CO3;
(2)能在空气中形成酸雨的气体SO2;
(3)含游离态氧元素的物质O2;
(4)医院常用0.9%的生理盐水,此盐水中的溶质是NaCl;
(5)能做食品干燥剂的物质是CaO;用化学方程式表示其原理CaO+H2O═Ca(OH)2.
| 元素名称 | 碳 | 氧 | 硫 | 氯 | 钠 | 钙 |
| 元素符号 | C | O | S | Cl | Na | Ca |
(2)能在空气中形成酸雨的气体SO2;
(3)含游离态氧元素的物质O2;
(4)医院常用0.9%的生理盐水,此盐水中的溶质是NaCl;
(5)能做食品干燥剂的物质是CaO;用化学方程式表示其原理CaO+H2O═Ca(OH)2.
18.下列物质的用途只是由其化学性质决定的是( )
0 169023 169031 169037 169041 169047 169049 169053 169059 169061 169067 169073 169077 169079 169083 169089 169091 169097 169101 169103 169107 169109 169113 169115 169117 169118 169119 169121 169122 169123 169125 169127 169131 169133 169137 169139 169143 169149 169151 169157 169161 169163 169167 169173 169179 169181 169187 169191 169193 169199 169203 169209 169217 211419
| A. | 石墨作电池的电极 | B. | 用氢气做燃料 | ||
| C. | 稀有气体充电发光 | D. | 用干冰做致冷剂 |






