题目内容
5.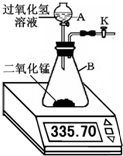 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 装置+过氧化氢溶液 +二氧化锰/g | 335.70 | 335.68 | 335.54 | 335.18 | 334.46 | 334.10 | 334.10 |
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.
分析 ①根据质量守恒定律,反应前即时间为0时烧瓶及所盛物质总质量与完全反应后即不再产生气体时间为5min时烧瓶及所盛物质总质量的差,即为反应放出气体氧气的质量;
②根据过氧化氢在二氧化锰催化下分解生成水和氧气的化学方程式,由生成氧气的质量计算出反应消耗过氧化氢的质量.
解答 解:①根据质量守恒定律可以知道:烧瓶及所剩余物质的总质量为332.50g,反应前后的质量差即为放出氧气的质量,反应生成氧气质量=335.70g-334.10g=1.6g,即生成氧气的质量为1.6,其物质的量为:$\frac{1.6g}{32g/mol}$=0.05mol;
②设过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}$=$\frac{32}{1.6g}$
x=3.4g
故答案为:(1)0.05;
(2)3.4g.
点评 根据质量守恒定律可以知道,天平的读数随反应时间的增加越来越小是由于反应不断放出气体氧气所致,待读数不变时,说明已完全反应,不再产生气体.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
15.北京时间2015年10月5日下午17时30分,“诺贝尔生理学或医学奖”获奖名单揭晓,中国女医药学家屠呦呦因发现青蒿素(青蒿素的化学式:C15H22O5)获奖,它是一种用于治疗疟疾的药物,下列有关青蒿素的说法错误的是( )
| A. | 青蒿素由碳、氢、氧三种元素组成 | |
| B. | 一个青蒿素分子是由15个碳原子、22个氢原子和5个氧原子构成 | |
| C. | 青蒿素中碳、氧元素的质量比为3:1 | |
| D. | 青蒿素中氢元素的质量分数最小 |
13.寒冷的冬天,户外的人呼吸时能看到“白气”,除了温度低这个原因外,同时也说明人呼出的气体中含有较多的( )
| A. | 二氧化碳 | B. | 氮气 | C. | 空气 | D. | 水蒸气 |
20.用表中的元素组成适当的物质(用化学式填空),回答下列问题:
(1)引起温室效应的主要物质是H2CO3;
(2)能在空气中形成酸雨的气体SO2;
(3)含游离态氧元素的物质O2;
(4)医院常用0.9%的生理盐水,此盐水中的溶质是NaCl;
(5)能做食品干燥剂的物质是CaO;用化学方程式表示其原理CaO+H2O═Ca(OH)2.
| 元素名称 | 碳 | 氧 | 硫 | 氯 | 钠 | 钙 |
| 元素符号 | C | O | S | Cl | Na | Ca |
(2)能在空气中形成酸雨的气体SO2;
(3)含游离态氧元素的物质O2;
(4)医院常用0.9%的生理盐水,此盐水中的溶质是NaCl;
(5)能做食品干燥剂的物质是CaO;用化学方程式表示其原理CaO+H2O═Ca(OH)2.
10.豆浆被称为“植物奶”,其中含有的异黄酮“C15H10O2)具有防癌功能,下列说法正确的是( )
| A. | 异黄酮中共含有27个原子 | |
| B. | 异黄酮中碳元素质量分数最大 | |
| C. | 异黄酮中C、H、O三种元素的质量比为15:10:2 | |
| D. | 异黄酮的化学式量为222g |
14.下列关于燃烧现象的描述,正确的是( )
| A. | 木炭在氧气中燃烧产生大量黑烟 | B. | 木炭在空气中燃烧发出白光 | ||
| C. | 镁条在空气中燃烧发出耀眼的白光 | D. | 铁丝在空气中剧烈燃烧,火星四射 |
15.下列物质中,属于纯净物的是( )
| A. | 纯牛奶 | B. | 冰水混合物 | C. | 纯净的空气 | D. | 稻花香白酒 |