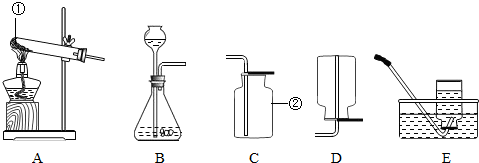
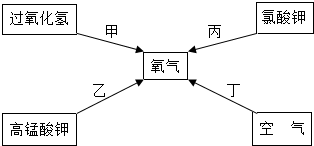
13.相同数目的下列原子,质量最小的是( )
| A. | 氢 | B. | 氧 | C. | 钠 | D. | 铁 |
12.已知质子数和中子数都是6的碳原子的质量为aKg,m个A原子的质量为bKg,则该原子的相对原子质量为( )
| A. | $\frac{12b}{a}$ | B. | $\frac{12a}{b}$ | C. | $\frac{b}{a}$ | D. | $\frac{12b}{ma}$ |
11.甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并 回答下列问题:
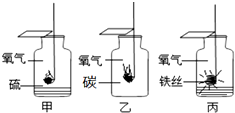
(1)甲、丙两实验集气瓶中均放少量水,其作用分别是,甲:吸收二氧化硫气体,防止污染空气,丙:防止生成的高温熔化物溅落炸裂瓶底;甲瓶中硫燃烧的表达式为硫+氧气$\stackrel{点燃}{→}$二氧化硫.
(2)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧,并将现象的记录在表中.
①小明实验前将铁丝绕成螺旋状的目的是增大铁丝与氧气的接触面积,便于铁丝燃烧;
③铁丝在氧气中燃烧的表达式是铁+氧气$\stackrel{点燃}{→}$四氧化三铁.

(1)甲、丙两实验集气瓶中均放少量水,其作用分别是,甲:吸收二氧化硫气体,防止污染空气,丙:防止生成的高温熔化物溅落炸裂瓶底;甲瓶中硫燃烧的表达式为硫+氧气$\stackrel{点燃}{→}$二氧化硫.
(2)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧,并将现象的记录在表中.
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 剧烈燃烧 火星四射 |
③铁丝在氧气中燃烧的表达式是铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
8.下列各物质中,前者是纯净物,后者是混合物的是( )
| A. | 洁净的空气、稀有气体 | B. | 液氧、红磷 | ||
| C. | 冰水共存物、自来水 | D. | 澄清石灰水、五氧化二磷 |
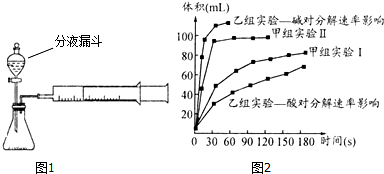
6.现甲、乙两化学小组安装两套如图1的相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)MnO2催化下H2O2分解的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)甲小组有如下实验设计方案,完成下表.
(4)甲、乙两小组得出如图2数据.
①甲组实验得出的数据可知:浓度越大,H2O2分解速率越快;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;乙组提出可以用Ba O2固体与硫酸溶液反应制H2 O2(已知还生成另一种物质),其化学反应方程式为BaO2+H2SO4=BaSO4↓+H2O2;支持这一方案的理是过氧化氢在酸性环境下分解较慢.
0 167680 167688 167694 167698 167704 167706 167710 167716 167718 167724 167730 167734 167736 167740 167746 167748 167754 167758 167760 167764 167766 167770 167772 167774 167775 167776 167778 167779 167780 167782 167784 167788 167790 167794 167796 167800 167806 167808 167814 167818 167820 167824 167830 167836 167838 167844 167848 167850 167856 167860 167866 167874 211419

(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)MnO2催化下H2O2分解的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)甲小组有如下实验设计方案,完成下表.
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
①甲组实验得出的数据可知:浓度越大,H2O2分解速率越快;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;乙组提出可以用Ba O2固体与硫酸溶液反应制H2 O2(已知还生成另一种物质),其化学反应方程式为BaO2+H2SO4=BaSO4↓+H2O2;支持这一方案的理是过氧化氢在酸性环境下分解较慢.
 甲、乙、丙、丁是常见的化合物,它们有如右图所示转化关系(部分物质已略去).甲是相对分子质量为16的有机物;乙是最常见的溶剂;丁是白色难溶固体,其中金属元素的质量分数为40%.则甲的化学式为CH4;反应②③的化学方程式分别为CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+2HCl=CaCl2+H2O+CO2↑;试剂A 中溶质在生产或生活中的一种用途是改良酸性土壤.
甲、乙、丙、丁是常见的化合物,它们有如右图所示转化关系(部分物质已略去).甲是相对分子质量为16的有机物;乙是最常见的溶剂;丁是白色难溶固体,其中金属元素的质量分数为40%.则甲的化学式为CH4;反应②③的化学方程式分别为CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+2HCl=CaCl2+H2O+CO2↑;试剂A 中溶质在生产或生活中的一种用途是改良酸性土壤.