6.下列对如图所示实验的分析正确的是( )
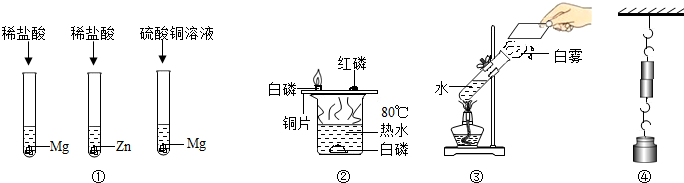

| A. | ①通过实验可以判断三种金属的活动性顺序为Mg、Zn、Cu | |
| B. | ②通过铜片上白磷、红磷的现象,说明燃烧需要氧气 | |
| C. | ③试管口出现白雾,管内的气体对塞子做功内能减少 | |
| D. | ④端面磨平的铅块压紧后能吊住大钩码,说明分子在不停地做无规则运动 |
5.从分子的角度分析敞口容器中的酒精逐渐减少的原因是( )
| A. | 分子体积很小 | B. | 分子间有间隔 | ||
| C. | 分子总在不断运动 | D. | 分子是由原子构成的 |
4.根据图中的有关信息判断,下列说法错误的是( )


| A. | 钠原子的核电荷数为11 | B. | 氯元素的原子序数X=17 | ||
| C. | 钠离子的最外层电子数为1 | D. | 氯原子的相对原子质量为35.45 |
3.暑假结束后,小丽带着快乐的心情返回学校,当好来到实验室时,意外实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了好的探究欲望.
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小丽的猜想:NaOH溶液部分部分变质.(1)你的新猜想:NaOH溶液全部变质.
【实验探究】小丽设计如下实验来验证自己的猜想,请根据表中内容填写小丽实验时的现象.
【实验反思】(4)实验方案中氯化钙溶液的量必须要足量,其原因是使溶液中的碳酸钠完全反应;
(5)下列物质:①BaCl2溶液;②Ca(NO3)2溶液;③Ca(OH)2溶液;④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是③④(填序号);
(6)小丽第二次滴加的试剂除用指示剂,还可以用硫酸铜溶液替代;
【拓展应用】(7)保存NaOH溶液的方法是密封保存.
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小丽的猜想:NaOH溶液部分部分变质.(1)你的新猜想:NaOH溶液全部变质.
【实验探究】小丽设计如下实验来验证自己的猜想,请根据表中内容填写小丽实验时的现象.
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液;然后再滴加酚酞试液 | (2)产生白色沉淀 (3)酚酞试液变红 | NaOH溶液部分变质 |
(5)下列物质:①BaCl2溶液;②Ca(NO3)2溶液;③Ca(OH)2溶液;④Ba(OH)2溶液,不能替代小丽实验中CaCl2溶液的是③④(填序号);
(6)小丽第二次滴加的试剂除用指示剂,还可以用硫酸铜溶液替代;
【拓展应用】(7)保存NaOH溶液的方法是密封保存.
2.推理是学习化学的一种重要方法,以下类推正确的是( )
| A. | 由同种分子构成的物质一定是纯净物,所以纯净物一定是由同种分子构成的 | |
| B. | 单质是由同种元素组成,所以由同种元素组成的纯净物一定是单质 | |
| C. | 碳酸盐与稀盐酸反应生成气体,所以与稀盐酸反应生成气体的物质一定是碳酸盐 | |
| D. | 在化学反应中,一氧化碳和氢气都能夺取氧化铜中的氧,所以一氧化碳和氢气都具有还原性 |
1.PM(particulate matter颗粒物)2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物.严重污染空气,造成阴霾天气,危害居民呼吸系统健康,因此成为影响空气质量的重要因素.根据你所学的知识,下列几个因素中不会影响空气质量,不会造成空气污染的是( )
0 167319 167327 167333 167337 167343 167345 167349 167355 167357 167363 167369 167373 167375 167379 167385 167387 167393 167397 167399 167403 167405 167409 167411 167413 167414 167415 167417 167418 167419 167421 167423 167427 167429 167433 167435 167439 167445 167447 167453 167457 167459 167463 167469 167475 167477 167483 167487 167489 167495 167499 167505 167513 211419
| A. | 可吸入颗粒物 | B. | 二氧化硫 | C. | 氮氧化物 | D. | 二氧化碳 |


 某化学学习小组做如图所示的实验,测定空气中氧气的含量.
某化学学习小组做如图所示的实验,测定空气中氧气的含量.