15.有10克氧化铜、氢氧化铜、硫酸铜的混合物与100克9.8%的稀硫酸恰好完全反应,则反应后所得溶液中的溶质质量可能为( )
| A. | 17克 | B. | 18克 | C. | 19克 | D. | 22克 |
11.聚合硫酸铁的化学式为[Fea(OH)b(SO4)c]m.取一定量的聚合硫酸铁样品与足量的稀盐酸反应,将反应后所得溶液平均分成两份,一份溶液中加入足量的氯化钡溶液,得到白色沉淀2.33克,另一份溶液加入足量的氢氧化钠溶液,过滤、洗涤、灼烧,得到氧化铁固体0.64克,则该聚合硫酸铁样品中b:c的比值为( )
| A. | 2:1 | B. | 3:1 | C. | 2:5 | D. | 4:5 |
9.现在有10克铁、锌和氧化镁的混合物,与X克7.3%的稀盐酸恰好完全反应,产生氢气0.2克,则X可能为( )
| A. | 200 | B. | 150 | C. | 73 | D. | 173 |
8.现有四瓶失去标签的无色溶液,分别是Ca(OH)2,KCl,Na2CO3,HCl溶液中的一种,已知甲可以和丙反应,也可以和丁反应.则下列说法中,正确的是( )
0 166200 166208 166214 166218 166224 166226 166230 166236 166238 166244 166250 166254 166256 166260 166266 166268 166274 166278 166280 166284 166286 166290 166292 166294 166295 166296 166298 166299 166300 166302 166304 166308 166310 166314 166316 166320 166326 166328 166334 166338 166340 166344 166350 166356 166358 166364 166368 166370 166376 166380 166386 166394 211419
| A. | 甲不可能是KCl | B. | 丙不一定是Ca(OH)2 | C. | 乙可能是HCl | D. | 丁一定是Na2CO3 |
 (1)材料是人类赖以生存和发展的重要物质基础.
(1)材料是人类赖以生存和发展的重要物质基础.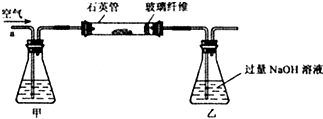
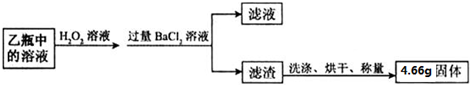
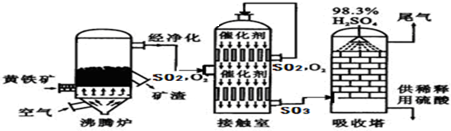
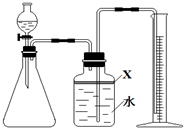 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验. 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: