9.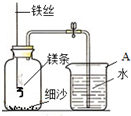 探究一:某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
探究一:某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
(1)燃烧、冷却后打开止水夹,水能进入集气瓶的原因是瓶内气体减少,导致压强减小,水沿导管进入瓶内.
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中还一定有氮气.
【发现问题】该气体是怎样减少的呢?
【假设】该气体与镁条反应而减少.
【查阅资料】镁条是一种化学性质比较活泼的金属,在氮气中能燃烧,产物为氮化镁(Mg3N2),镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁.
【交流与反思】集气瓶中放少量细沙的目的是防止集气瓶炸裂,产物氮化镁的状态应为固态.
探究二:以下是该小组探究影响H2O2溶液反应速率部分因素的相关实验数据.
(1)写出实验室用H2O2溶液和MnO2混合制氧气的符号表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)通过实验①和②对比可知,化学反应速率与反应物浓度(或浓度)有关;
从实验③和④对比可知,化学反应速率与温度的关系是:温度越高,化学反应速率越快.
(3)通过上述实验能(填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率.
 探究一:某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
探究一:某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.(1)燃烧、冷却后打开止水夹,水能进入集气瓶的原因是瓶内气体减少,导致压强减小,水沿导管进入瓶内.
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中还一定有氮气.
【发现问题】该气体是怎样减少的呢?
【假设】该气体与镁条反应而减少.
【查阅资料】镁条是一种化学性质比较活泼的金属,在氮气中能燃烧,产物为氮化镁(Mg3N2),镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁.
【交流与反思】集气瓶中放少量细沙的目的是防止集气瓶炸裂,产物氮化镁的状态应为固态.
探究二:以下是该小组探究影响H2O2溶液反应速率部分因素的相关实验数据.
| 实验序号 | H2O2溶液浓度% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
(2)通过实验①和②对比可知,化学反应速率与反应物浓度(或浓度)有关;
从实验③和④对比可知,化学反应速率与温度的关系是:温度越高,化学反应速率越快.
(3)通过上述实验能(填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率.
5.下列不属于缓慢氧化的是( )
| A. | 蜡烛缓慢地燃烧 | B. | 食物的腐烂 | C. | 酿酒酿醋 | D. | 钢铁生锈 |
4.下列说法正确的是( )
0 165391 165399 165405 165409 165415 165417 165421 165427 165429 165435 165441 165445 165447 165451 165457 165459 165465 165469 165471 165475 165477 165481 165483 165485 165486 165487 165489 165490 165491 165493 165495 165499 165501 165505 165507 165511 165517 165519 165525 165529 165531 165535 165541 165547 165549 165555 165559 165561 165567 165571 165577 165585 211419
| A. | 氧气支持燃烧,常作宇宙航行中的重要燃料 | |
| B. | 因为氧气与氮气的密度不同,所以工业上分离液态空气法制取氧气 | |
| C. | 木炭在空气中燃烧不如氧气中剧烈,因为空气中氧气含量较低 | |
| D. | 鱼、虾等能在水中生存,是由于氧气易溶于水 |
 铁及其化合物在日常生活中随处可见.
铁及其化合物在日常生活中随处可见.