11.下列各组溶液,不用其他试剂不能鉴别出来的是( )
| A. | H2SO4 Na2CO3 NaCl KNO3 | B. | BaCl2 Na2SO4 Na2CO3 HCl | ||
| C. | NaOH Na2CO3 酚酞 CaCl2 | D. | CuSO4 NaOH BaCl2 NaCl |
10.下列说法正确的是( )
| A. | 实验证明氢氧化钠是否变质,加入一滴稀盐酸,没有观察到气泡说明没有变质 | |
| B. | 鸡蛋清加入某盐溶液,有固体析出,蛋白质不一定变性 | |
| C. | 高炉炼铁中所需的高温和一氧化碳的生成都与焦炭有关 | |
| D. | 某化肥中加熟石灰研磨,未闻到氨臭味,该化肥一定不是氮肥 |
9.2015年地球一小时于3月28日晚8:30举行.为响应全球应对气候变化的主题,今年地球一小时在中国将继续聚焦当前最急迫、最受关注的环境议题--雾霾,发出“能见蔚蓝”的倡议.作为中学生不符合这一主题的做法是( )
| A. | 选择自行车和公交车作为出行工具 | |
| B. | 将废纸、汽水瓶等收集起来,一次性焚烧 | |
| C. | 让衣服自然晾干,节约用纸,不使用一次性塑料袋 | |
| D. | 拒绝使用一次性木筷,用电子贺卡代替纸质贺卡 |
8.KOH溶液中含有H2O、K+、OH-、能使无色酚酞试液变成红色.某化学兴趣小组想探究KOH溶液使无色酚酞试液变成红色的原因.
【提出问题】KOH溶液中的什么成分使无色酚酞试液变红?
【猜想】猜想1:KOH溶液中的H2O使无色酚酞试液变红.
猜想2:KOH溶液中的K+使无色酚酞试液变红.
猜想3:KOH溶液中的OH-(填化学式)使无色酚酞试液变红.
【实验探究】
补充上面表格所缺的地方:
(1):用试管取少量KOH溶液 (2):试管内溶液不变色 (3):猜想3成立
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学理由无色酚酞试液中含有水.
【拓展】①向Ba(OH)2溶液中滴入几滴无色酚酞试液,观察到的现象是无色酚酞试液变红色;
②KOH固体应密封保存.
【提出问题】KOH溶液中的什么成分使无色酚酞试液变红?
【猜想】猜想1:KOH溶液中的H2O使无色酚酞试液变红.
猜想2:KOH溶液中的K+使无色酚酞试液变红.
猜想3:KOH溶液中的OH-(填化学式)使无色酚酞试液变红.
【实验探究】
| 实验操作 | 反应② 实验现象 | 结论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液 | 试管内溶液不变色 | 猜想1不成立 |
| ②用试管取少量KCl溶液,滴入1-2滴无色酚酞试液 | 试管内溶液不变色 | 猜想2不成立 |
| ③用试管取少量KOH溶液,滴入1-2滴无色酚酞试液 | 试管内溶液变红 | 猜想3成立 |
(1):用试管取少量KOH溶液 (2):试管内溶液不变色 (3):猜想3成立
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学理由无色酚酞试液中含有水.
【拓展】①向Ba(OH)2溶液中滴入几滴无色酚酞试液,观察到的现象是无色酚酞试液变红色;
②KOH固体应密封保存.
7.一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,是当前使用最为广泛的洗涤助剂之一.某校化学兴趣小组的同学在老师的指导下对该产品开展了以下探究活动.
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
【实验探究二】过碳酸钠的含量测定
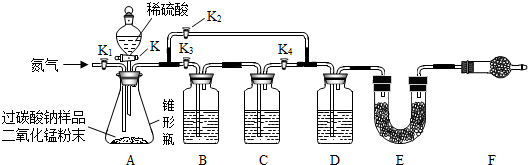
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).
【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K、K2,直到反应不再进行;⑥再次称量装置E的质量.以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置C的作用是检验空气中的二氧化碳是否除尽;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是使反应产生的二氧化碳全部被碱石灰吸收.
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,该样品中过碳酸钠的含量为92%.
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水、振荡 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向该试管中加入适量的二氧化锰粉末 | 有大量气泡 产生 | |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 过碳酸钠溶于水能生成过氧化氢.过氧化氢分解,产生的气体是氧气 |
| ④ | 取试管中的上层清液加入氯化钙溶液 | 产生白色沉淀 | 过碳酸钠溶于水能生成碳酸钠. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O=Na2CO3+H2O2. | ||
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).

【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K、K2,直到反应不再进行;⑥再次称量装置E的质量.以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置C的作用是检验空气中的二氧化碳是否除尽;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是使反应产生的二氧化碳全部被碱石灰吸收.
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,该样品中过碳酸钠的含量为92%.
5. 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
(1)甲同学的实验中向稀盐酸中滴加石蕊试液后,溶液颜色为红色.
(2)甲同学将两支试管中的液体混合后,烧杯A溶液中的溶质有BC.
A.HClB.NaOHC.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
①NaCl和NaOH,②NaOH、NaCl、Na2CO3,③NaOH、NaCl、Ca(OH)2.
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
(4)最后,两位同学向烧杯C中加入适量的稀盐酸,实现了此次实验的绿色排放(呈中性).
0 164212 164220 164226 164230 164236 164238 164242 164248 164250 164256 164262 164266 164268 164272 164278 164280 164286 164290 164292 164296 164298 164302 164304 164306 164307 164308 164310 164311 164312 164314 164316 164320 164322 164326 164328 164332 164338 164340 164346 164350 164352 164356 164362 164368 164370 164376 164380 164382 164388 164392 164398 164406 211419
 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.(1)甲同学的实验中向稀盐酸中滴加石蕊试液后,溶液颜色为红色.
(2)甲同学将两支试管中的液体混合后,烧杯A溶液中的溶质有BC.
A.HClB.NaOHC.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
①NaCl和NaOH,②NaOH、NaCl、Na2CO3,③NaOH、NaCl、Ca(OH)2.
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
| 操作方法 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,向其中滴加足量的稀盐酸 ②取少量滤液于试管中,向其中加入碳酸钠溶液 ③取两只试管,分别加入少量的滤液,分别滴加足量的稀盐酸和碳酸钠溶液 | 有气泡产生 有沉淀产生 以上两只试管均无现象 | 则C中的废液成分是NaOH、NaCl、Na2CO3 则C中的废液成分是NaOH、NaCl、Ca(OH)2 则C中的废液成分是NaOH、NaCl |
 已知A-E是初中化学的常见物质.B是一种钠盐;胃液中含有适量的C,可帮助消化;它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)请回答:
已知A-E是初中化学的常见物质.B是一种钠盐;胃液中含有适量的C,可帮助消化;它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)请回答:


