13.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 加入盐酸,有无色气体产生的物质中一定含有碳酸盐 | |
| B. | 有机物中一定含碳元素,因此含有碳元素的化合物一定是有机物 | |
| C. | 向某无色溶液中滴加酚酞,酚酞变红,该溶液一定是碱溶液 | |
| D. | 某物质在氧气中燃烧能生成水,该物质中一定含有氢元素 |
12.绿茶中含有单宁酸,它具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法中正确的是( )
| A. | 单宁酸由76个碳原子、52个氢原子和46个氧原子构成 | |
| B. | 单宁酸属于有机高分子化合物 | |
| C. | 单宁酸分子中氢、氧原子个数比为26:23 | |
| D. | 单宁酸分子由碳元素、氢元素和氧元素组成 |
11.下列实验操作中错误的是( )
| A. |  闻气味方法 | B. | 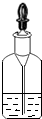 滴管用后不洗涤直接放回原瓶 | ||
| C. | 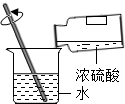 稀释浓硫酸 | D. |  称量氢氧化钠质量 |
10.下列属于物理变化的是( )
| A. | 蜡烛燃烧 | B. | 用糯米等原料做甜酒酿 | ||
| C. | 分离液态空气制氧气 | D. | 用小苏打、柠檬酸等制汽水 |
9.下列属于纯净物的是( )
| A. | 钢 | B. | 矿泉水 | C. | 干冰 | D. | 过氧化氢溶液 |
7.过氧化钠(Na2O2)可用作潜水艇有呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某化学研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中的水或二氧化碳反应生成氧气.
2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2
【提出问题】这瓶过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:你还能提出的假设是过氧化钠全部变质;
【实验探究1】请你设计实验方案验证上面的猜想.
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究2】小东取部分固体于试管中,加入适量水溶解,然后再加入足量的氧化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,游溶液变红则说明变质的过氧化钠中含有氢氧化风钠.
【定性分析】
(1)由【实验探究2]可以确定在加入氯化钙溶液前,溶液中含有的溶质是NaOH、Na2CO3(填化学式).
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【定量研究】称取6.04g的过氧化钠样品于锥形瓶中,加入足量的蒸馏水,共收集到气体0.64g,再向上述锥形瓶中加入足量的澄清石灰水,充分反应后,经过沉淀、过滤、干燥等,得到固体2.00g.
(1)写出加入石灰水后的化学反应方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)6.04g上述样品中,含有氢氧化钠的质量是0.8g.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式).
0 163755 163763 163769 163773 163779 163781 163785 163791 163793 163799 163805 163809 163811 163815 163821 163823 163829 163833 163835 163839 163841 163845 163847 163849 163850 163851 163853 163854 163855 163857 163859 163863 163865 163869 163871 163875 163881 163883 163889 163893 163895 163899 163905 163911 163913 163919 163923 163925 163931 163935 163941 163949 211419
【查阅资料】过氧化钠能与空气中的水或二氧化碳反应生成氧气.
2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2
【提出问题】这瓶过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:你还能提出的假设是过氧化钠全部变质;
【实验探究1】请你设计实验方案验证上面的猜想.
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| (1) | 假设1成立 | ||
| (2) | 假设2成立 | ||
| (3) | 假设3成立 |
【实验探究2】小东取部分固体于试管中,加入适量水溶解,然后再加入足量的氧化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,游溶液变红则说明变质的过氧化钠中含有氢氧化风钠.
【定性分析】
(1)由【实验探究2]可以确定在加入氯化钙溶液前,溶液中含有的溶质是NaOH、Na2CO3(填化学式).
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【定量研究】称取6.04g的过氧化钠样品于锥形瓶中,加入足量的蒸馏水,共收集到气体0.64g,再向上述锥形瓶中加入足量的澄清石灰水,充分反应后,经过沉淀、过滤、干燥等,得到固体2.00g.
(1)写出加入石灰水后的化学反应方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)6.04g上述样品中,含有氢氧化钠的质量是0.8g.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式).
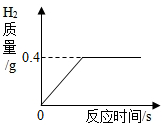 现有一块质量为20克的铜锌合金,将它投入到100克稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试计算:
现有一块质量为20克的铜锌合金,将它投入到100克稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试计算: 目前,电动车以其小巧轻便而成为普通市民的代步工具(如图所示).
目前,电动车以其小巧轻便而成为普通市民的代步工具(如图所示). ”表示碳原子、“○”表示氧原子,根据图2回答下列问题:
”表示碳原子、“○”表示氧原子,根据图2回答下列问题:
 我市银滩是国家“AAAA”级滨海旅游度假区,有漫长的海岸线,海洋资源十分丰富,海水中含有大量的化学物质.
我市银滩是国家“AAAA”级滨海旅游度假区,有漫长的海岸线,海洋资源十分丰富,海水中含有大量的化学物质.