题目内容
8.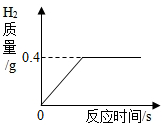 现有一块质量为20克的铜锌合金,将它投入到100克稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试计算:
现有一块质量为20克的铜锌合金,将它投入到100克稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试计算:(1)完全反应后生成H2的质量为0.4克;
(2)该铜锌合金中含铜的质量分数是多少?
(3)所用硫酸溶液中溶质的质量分数是多少?
分析 铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气;
根据图中数据可以判断生成氢气的质量,根据氢气的质量可以计算锌的质量和反应的硫酸的质量,进一步可以计算该铜锌合金中含铜的质量分数和所用硫酸溶液中溶质的质量分数.
解答 解:(1)由图中数据可知,完全反应后生成氢气的质量为0.4g.
故填:0.4.
(2)设锌的质量为x,硫酸的质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.4g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.4g}$,
x=13g,y=19.6g,
该铜锌合金中含铜的质量分数=$\frac{20g-13g}{20g}$×100%=35%,
答:该铜锌合金中含铜的质量分数是35%.
(3)所用硫酸溶液中溶质的质量分数=$\frac{19.6g}{100g}$×100%=19.6%,
答:所用硫酸溶液中溶质的质量分数是19.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
18.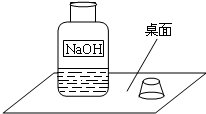 一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
(1)此情此景你首先想到的是它可能变质了,该变质反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
(2)围绕此瓶NaOH溶液是否变质的问题,小娟展开了探究活动.
①取少量溶液于试管中,滴加稀盐酸,有气泡产生,可以证明NaOH溶液已经变质.
②欲证明变质的溶液中尚存NaOH,请你帮助小娟完成以下探究方案:
(3)根据以上探究结果,你认为实验室对氢氧化钠应密封保存.
 一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).(1)此情此景你首先想到的是它可能变质了,该变质反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
(2)围绕此瓶NaOH溶液是否变质的问题,小娟展开了探究活动.
①取少量溶液于试管中,滴加稀盐酸,有气泡产生,可以证明NaOH溶液已经变质.
②欲证明变质的溶液中尚存NaOH,请你帮助小娟完成以下探究方案:
| 探究目的 | 探究步骤 | 预计现象 |
| 除尽溶液中的CO32- | ①:取少量溶液于试管中,滴加足量的氯化钙溶液试剂 | 产生白色沉淀 |
| 证明溶液中尚存NaOH | ②:向实验①所得溶液中滴加酚酞试液 | 溶液变红 |
3.我国科学家利用石墨稀(一种由碳原子构成的物质)与铝合金,研制出一种具备特殊性能的烯合金,下列对烯合金和石墨烯的说法错误的是( )
| A. | 石墨烯在一定条件下能氧气反应 | B. | 烯合金是混合物 | ||
| C. | 烯合金具有优良的导电性 | D. | 石墨烯在常温下化学性质活泼 |
13.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 加入盐酸,有无色气体产生的物质中一定含有碳酸盐 | |
| B. | 有机物中一定含碳元素,因此含有碳元素的化合物一定是有机物 | |
| C. | 向某无色溶液中滴加酚酞,酚酞变红,该溶液一定是碱溶液 | |
| D. | 某物质在氧气中燃烧能生成水,该物质中一定含有氢元素 |
20.小刚同学根据所学化学知识,向家人提出了如下建议,其中不合理的是( )
| A. | 霉变的大米蒸熟后食用无害 | B. | 用灼烧的方法能鉴别绦纶和羊毛 | ||
| C. | 用食醋除去水壶中的水垢 | D. | 用加热煮沸的方法降低水的硬度 |
17.下列物质中含有氧气的是( )
| A. | MnO2 | B. | KClO3 | C. | 氯化镁 | D. | 空气 |

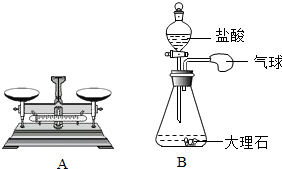 探究化学反应前后物质的总质量有无变化的实验方案有多种.小东同学利用大理石(主要成分CaCO3)和盐酸(HCl)反应及如图所示的仪器和装置,来探究化学反应前后物质的总质量有无变化.经查阅资料知,大理石和盐酸反应生成二氧化碳气体、水和氯化钙(CaCl2).请你回答下列问题:
探究化学反应前后物质的总质量有无变化的实验方案有多种.小东同学利用大理石(主要成分CaCO3)和盐酸(HCl)反应及如图所示的仪器和装置,来探究化学反应前后物质的总质量有无变化.经查阅资料知,大理石和盐酸反应生成二氧化碳气体、水和氯化钙(CaCl2).请你回答下列问题: