2.如表是某学校实验室从买回的浓硫酸试剂的标签上的部分内容,阅读后计算:
(1)该试剂瓶中浓硫酸溶液的质量是多少克?
(2)现要将100g这种浓硫酸稀释为溶质质量分数为20%的稀硫酸,需要加入多少mL水?(水的密度为1g/mL)
(3)用量筒量取所需体积的水时,俯视刻 度,则稀硫酸的溶质质量分数将偏大.(偏大或偏填小)
| 浓硫酸(H2SO4)500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 |
(2)现要将100g这种浓硫酸稀释为溶质质量分数为20%的稀硫酸,需要加入多少mL水?(水的密度为1g/mL)
(3)用量筒量取所需体积的水时,俯视刻 度,则稀硫酸的溶质质量分数将偏大.(偏大或偏填小)
20. 如图是甲、乙两物质的溶解度曲线,由溶解度曲线得出以下几条信息,正确的是( )
如图是甲、乙两物质的溶解度曲线,由溶解度曲线得出以下几条信息,正确的是( )
 如图是甲、乙两物质的溶解度曲线,由溶解度曲线得出以下几条信息,正确的是( )
如图是甲、乙两物质的溶解度曲线,由溶解度曲线得出以下几条信息,正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲物质的溶解度受温度变化的影响比乙大 | |
| C. | t2℃时,把30克甲溶解在100克水中,所得溶液为饱和溶液 | |
| D. | t1℃时,甲和乙的水溶液中溶质质量分数一定相等 |
19.下列除去杂质的方法中,错误的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 稀硫酸 | 铜 | 过滤 |
| B | CO2 | SO2 | 通入氢氧化钠后收集 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | CuSO4 | 稀硫酸 | 加入过量CuO粉末充分反应后、过滤 |
| A. | A | B. | B | C. | C | D. | D |
18.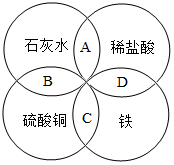 铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )
铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )
 铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )
铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )| A. | A无明显现象产生 | B. | B有红褐色沉淀 | ||
| C. | C有红色固体析出产生 | D. | D有气泡生成 |
15.地壳中含量最多的金属元素X与含量最多的非金属元素Y组成的化合物的分子式可能是-( )
| A. | XY2 | B. | X2Y3 | C. | XY | D. | X3Y4 |
14.下列物质的化学式,书写正确的是( )
| A. | 氯化铁FeCl2 | B. | 二铝化三氧 Al2O3 | ||
| C. | 三氧化四铁Fe3O4 | D. | 碳酸铵(NH4)2CO3 |
13.现有一瓶标签破损的试剂(如图).请你就该试剂的两种猜想,完成如表:
0 159111 159119 159125 159129 159135 159137 159141 159147 159149 159155 159161 159165 159167 159171 159177 159179 159185 159189 159191 159195 159197 159201 159203 159205 159206 159207 159209 159210 159211 159213 159215 159219 159221 159225 159227 159231 159237 159239 159245 159249 159251 159255 159261 159267 159269 159275 159279 159281 159287 159291 159297 159305 211419
| 猜想 | 实验过程 | 实验现象 | 结论 | |
| ①溶质是 Na2SO4 | 取少量该溶液于试管中, 滴入稀盐酸 | 无明显变化 | 猜想①不成立 |  |
| ②溶质是Na2CO3 | 取少量该溶液于试管中, 滴入稀盐酸将产生的气体通入澄清的石灰水中 | 有气泡产生澄清的石灰水变浑浊 | 猜想②成立; |
 同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.小红同学查阅资料获得了木糖醇和蔗糖的溶解度曲线,进行如下实验:向l00克60℃恒温的水中加入100克木糖醇,充分溶解后,所得的溶液是饱和 溶液(选填“饱和”或“不饱和”),该溶液的溶质质量分数为47.4%.
同学们都知道“木糖醇口香糖”吧?经研究表明木糖醇的甜度高,溶解性好,防龋齿,是一种理想的蔗糖替代品,适合糖尿病患者食用.小红同学查阅资料获得了木糖醇和蔗糖的溶解度曲线,进行如下实验:向l00克60℃恒温的水中加入100克木糖醇,充分溶解后,所得的溶液是饱和 溶液(选填“饱和”或“不饱和”),该溶液的溶质质量分数为47.4%.