7.硝酸是一种常见的酸,它与稀盐酸、稀硫酸化学性质是否完全相同呢?某化学小组对此很感兴趣,向老师提出探究硝酸的化学性质,老师高兴答应并带领同学们进行了硝酸某些化学性质的实验探究.
【猜想与假设】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变红色.
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入
稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红
棕色有刺激性气味的气体B.
【提出问题】(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成氢气.
(2)硝酸具有强氧化性,能使有色物质褪色.
(3)氮元素某些气态化合物的某些性质如下表:
【交流与讨论】(1)甲同学认为石蕊变色后又褪色的原因是硝酸具有强氧化性,使石蕊试液褪色.
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①乙同学认为A是N2,遭到大家的一致反对,原因是氮气的化学性质比较稳定,常温下不能被氧化成二氧化氮.
②丙同学认为A是NH3,也遭到大家的一致反对,原因是氨气极易溶于水,大多数气体会溶解在稀硝酸中,且常温下氨气不易
被氧化成二氧化氮.
(3)经讨论,最终大家获得了A是NO的共识.
【延伸与拓展】丁同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象.请完成Cu与稀HNO3反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O.
【猜想与假设】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变红色.
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入
稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红
棕色有刺激性气味的气体B.
【提出问题】(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成氢气.
(2)硝酸具有强氧化性,能使有色物质褪色.
(3)氮元素某些气态化合物的某些性质如下表:
| NH3 | NO | NO2 | |
| 颜色 | 无色 | 无色 | 红棕色 |
| 溶解性 | 极易溶于水 | 难溶于水 | 可溶于水或硝酸 |
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①乙同学认为A是N2,遭到大家的一致反对,原因是氮气的化学性质比较稳定,常温下不能被氧化成二氧化氮.
②丙同学认为A是NH3,也遭到大家的一致反对,原因是氨气极易溶于水,大多数气体会溶解在稀硝酸中,且常温下氨气不易
被氧化成二氧化氮.
(3)经讨论,最终大家获得了A是NO的共识.
【延伸与拓展】丁同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象.请完成Cu与稀HNO3反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O.
6.在盐酸除铁锈的实验中,常会发现生锈的铁钉表面有一些气泡产生.
【提出问题】气泡是怎么产生的?
【猜想假设】猜想1:铁和稀盐酸反应;猜想2:铁与水反应;猜想3:铁锈与水反应.
【实验过程】为了验证假设,某同学设计了如图甲所示的实验方案进行探究.
【反思】(1)有同学认为上述实验不够严谨,溶液中的水可能会对实验产生影响.于是他们又进行了如图乙的对照实验,试管3中发生的化学反应属于置换反应基本反应类型.
(2)还有同学想:气体会不会是铁锈与水反应产生的?他认为还要补充一个铁锈与水反应的实验,你觉得有没有必要?没有必要,原因是试管2中,稀盐酸中含有水,反应过程中不产生气泡,说明铁锈不能和水反应生成气体.

【提出问题】气泡是怎么产生的?
【猜想假设】猜想1:铁和稀盐酸反应;猜想2:铁与水反应;猜想3:铁锈与水反应.
【实验过程】为了验证假设,某同学设计了如图甲所示的实验方案进行探究.
| 甲 | 现象 | 结论 |
| 试管1 | 产生气泡 | 猜想(1)正确 |
| 试管2 | 不产生气泡 |
(2)还有同学想:气体会不会是铁锈与水反应产生的?他认为还要补充一个铁锈与水反应的实验,你觉得有没有必要?没有必要,原因是试管2中,稀盐酸中含有水,反应过程中不产生气泡,说明铁锈不能和水反应生成气体.
4.CO2的资源化利用日趋成为研究热点.
查阅资料:①CO2与H2能在催化剂表面反应生成CH4与H2O;②CH4在高温下能与CuO 反应,其反应的化学方程式为CH4+4CuO$\stackrel{△}{→}$4Cu+CO2+2H2O.
为探究上述反应,设计如下装置并进行实验.

查阅资料:①CO2与H2能在催化剂表面反应生成CH4与H2O;②CH4在高温下能与CuO 反应,其反应的化学方程式为CH4+4CuO$\stackrel{△}{→}$4Cu+CO2+2H2O.
为探究上述反应,设计如下装置并进行实验.

| 实验装置 | 实验现象 | 解释原理与结论 |
| B | 无现象 | 目的:吸收没有反应的二氧化碳 |
| C | 无现象 | 目的:吸收水蒸气 |
| D | 黑色固体变红色 | 可能是H2和CH4共同与CuO反应的结果,写出H2和CuO反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O |
| E | 白色固体变蓝色 | 不能(“能”或“不能”)说明H2与CuO发生化学反应. |
| F | 澄清石灰水变浑浊 | 能(“能”或“不能”)说明CH4与CuO发生化学反应. |
19.下列说法中正确的一项是( )
| A. | 可用浓硫酸干燥H2、NH3、Cl2等气体 | |
| B. | 向某溶液中加入BaCl2溶液出现白色沉淀,则该溶液中肯定有SO42- | |
| C. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 利用NaOH溶液可以鉴别Na2SO4、MgCl2和FeSO4三种溶液 |
18.在高空中有一层臭氧层,它吸收了太阳光中的绝大部分的紫外线,使地球上的生物免受紫外线的伤害.臭氧的化学式是O3,下列关于臭氧的说法正确的是( )
0 159079 159087 159093 159097 159103 159105 159109 159115 159117 159123 159129 159133 159135 159139 159145 159147 159153 159157 159159 159163 159165 159169 159171 159173 159174 159175 159177 159178 159179 159181 159183 159187 159189 159193 159195 159199 159205 159207 159213 159217 159219 159223 159229 159235 159237 159243 159247 159249 159255 159259 159265 159273 211419
| A. | 臭氧由3个氧元素组成 | B. | 臭氧由3个氧原子构成 | ||
| C. | 臭氧是单质 | D. | 臭氧是化合物 |

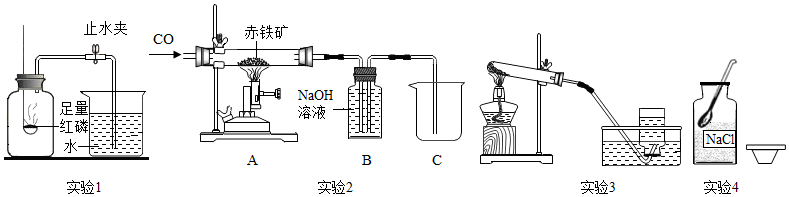

 化学实验操作的先后顺序和试剂的用量常常影响实验的结果.NaOH溶液和H2SO4溶液混合时没有明显现象,无法说明二者是否发生了反应.
化学实验操作的先后顺序和试剂的用量常常影响实验的结果.NaOH溶液和H2SO4溶液混合时没有明显现象,无法说明二者是否发生了反应.