13. 化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验.
化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验.
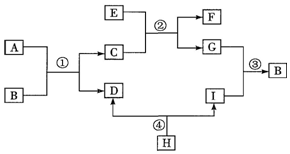
三个小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末.
A组:探究催化剂对化学反应速率的影响
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
由此可出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用,某同学对该结论提出疑问.
补充对比实验,操作为取5mL10%H2O2溶液,记录数据.
结果:长时间(大于100s),收集到很少量气体.
更正结论:红砖粉末有(选填“有”、“无”)催化作用,三者中二氧化锰催化效率最高.
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t1.
乙同学:取10mL2.5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t2.
实验结果t1<t2.
结论:浓度越大,反应速率越快.
丙同学:对实验设计提出疑问,并补充实验取10mL5%H2O2溶液,加入0.5gCuO为催化剂,进行实验,记录时间t3..
记录时间t3,且t1<t3<t2.
更正结论为:当催化剂相同时,反应物浓度越大,反应速率越快.
C组:探究温度对化学反应速率的影响.
取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴记录时间t4、t5,且t4>t5.
结论:当反应物浓度和催化剂相同时,温度越高,反应速率越快.
综上所述:①为了研究某一因素对化学反应速率的影响,必须只允许有一个变量,其他量必须相同.
②探究发现影响化学反应速率的因素有催化剂、反应物浓度、温度.
 化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验.
化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验.三个小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末.
A组:探究催化剂对化学反应速率的影响
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
| 试剂 | MnO2 | 红砖粉末 | CuO |
| t/s | 10 | 60 | 20 |
补充对比实验,操作为取5mL10%H2O2溶液,记录数据.
结果:长时间(大于100s),收集到很少量气体.
更正结论:红砖粉末有(选填“有”、“无”)催化作用,三者中二氧化锰催化效率最高.
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t1.
乙同学:取10mL2.5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t2.
实验结果t1<t2.
结论:浓度越大,反应速率越快.
丙同学:对实验设计提出疑问,并补充实验取10mL5%H2O2溶液,加入0.5gCuO为催化剂,进行实验,记录时间t3..
记录时间t3,且t1<t3<t2.
更正结论为:当催化剂相同时,反应物浓度越大,反应速率越快.
C组:探究温度对化学反应速率的影响.
取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴记录时间t4、t5,且t4>t5.
结论:当反应物浓度和催化剂相同时,温度越高,反应速率越快.
综上所述:①为了研究某一因素对化学反应速率的影响,必须只允许有一个变量,其他量必须相同.
②探究发现影响化学反应速率的因素有催化剂、反应物浓度、温度.
12.工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe2O4.
【查阅资料】1.草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O$\frac{\underline{\;H_{2}SO_{4}\;}}{△}$CO2↑+CO↑+4H2O.
2.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳.
3.铁的常见氧化物中铁的质量分数:
【问题讨论】为了测定铁红中铁的质量分数,小组同学进行如下实验.(装置气密性良好)
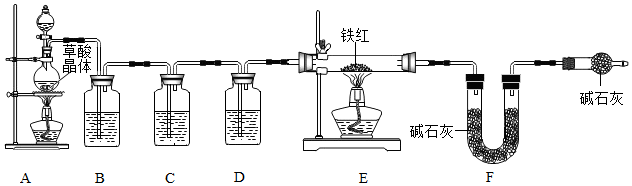
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是cba.(填字母序号)
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(2)C装置的作用是检验二氧化碳是否除尽.
(3)写出E装置中所发生反应的一个化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(或4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2或CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2).
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①若E中充分反应后得到铁粉的质量为mg,则7.0<m<7.78.
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是72%.
【实验反思】
(1)如果缺少装置G(不考虑其他因素),则测得样品中铁的质量分数会偏小(选填“偏小”“不变”或“偏大”).
(2)该实验装置的一个明显缺陷是缺少尾气处理装置.
【查阅资料】1.草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O$\frac{\underline{\;H_{2}SO_{4}\;}}{△}$CO2↑+CO↑+4H2O.
2.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳.
3.铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |

(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是cba.(填字母序号)
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(2)C装置的作用是检验二氧化碳是否除尽.
(3)写出E装置中所发生反应的一个化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(或4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2或CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2).
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①若E中充分反应后得到铁粉的质量为mg,则7.0<m<7.78.
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是72%.
【实验反思】
(1)如果缺少装置G(不考虑其他因素),则测得样品中铁的质量分数会偏小(选填“偏小”“不变”或“偏大”).
(2)该实验装置的一个明显缺陷是缺少尾气处理装置.
9.某纯净物X在空气中燃烧,反应的化学方程式为:3X+2O2$\frac{\underline{\;点燃\;}}{\;}$2CO+CO2+3H2O,则X的化学式为( )
| A. | CH2O | B. | CH4O | C. | C3H6 | D. | CH2O2 |
8.化学与人体健康密切相关.市场上有“高钙牛奶”、“加氟牙膏”、“葡萄糖酸锌”等商品,这里的钙、氟、
锌应理解为( )
锌应理解为( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 离子 |
7.下列生活用品不属于有机合成材料的是( )
| A. | 塑料瓶 | B. | 不锈钢刀 | C. | 涤纶布料 | D. | 汽车轮胎 |
6.下列现象属于化学变化的是( )
| A. | 碘溶于酒精制成碘酒 | B. | 石蜡熔化 | ||
| C. | 以石墨为原料合成金刚石 | D. | 汽油挥发 |
5.下列物质都属于纯净物的一组是( )
①冰水混合物 ②洁净的空气 ③液氮 ④石灰水.
0 158208 158216 158222 158226 158232 158234 158238 158244 158246 158252 158258 158262 158264 158268 158274 158276 158282 158286 158288 158292 158294 158298 158300 158302 158303 158304 158306 158307 158308 158310 158312 158316 158318 158322 158324 158328 158334 158336 158342 158346 158348 158352 158358 158364 158366 158372 158376 158378 158384 158388 158394 158402 211419
①冰水混合物 ②洁净的空气 ③液氮 ④石灰水.
| A. | ②④ | B. | ①③ | C. | ①② | D. | ③④ |