我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )
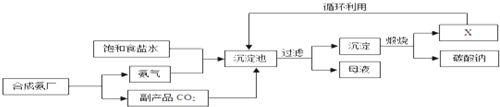

| A、沉淀池中的反应物共含有五种元素 | B、过滤得到的“母液”中一定只含有两种溶质 | C、图中X可能是氨气 | D、通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
“NaCl+CO2+NH3+H2O═NaHCO3+NaCl”是氨碱法制纯碱中的重要反应.下列相关认识中,不正确的是( )
| A、在加压的条件下向饱和氨盐水中通CO2,更有利于反应的发生 | B、析出晶体后的溶液是NaHCO3的饱和溶液 | C、该条件下NaHCO3的溶解度比NH4Cl的大,所以NaHCO3先结晶析出 | D、析出晶体后剩余溶液中含有两种溶质 |
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )


| A、沉淀池中的反应物共含有七种元素 | B、过滤得到的“母液”中一定只含有两种溶质 | C、图中X可能是氨气 | D、通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
“NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl”是著名的“侯氏制碱法”的重要反应,反应生成的NaHCO3(一种盐)达到一定浓度时会从溶液中先结晶出来.下面是4位同学对该反应涉及的有关知识发表的部分见解,其中正确的是( )
| A、这个反应属于复分解反应 | B、NaHCO3一定是难溶于水的物质 | C、反应后的溶液中存在NH4+ | D、结晶出NaHCO3后的溶液中没有Na+ |
工业上采用氨碱法生产纯碱的原理是:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl,先向饱和食盐水中通入较多NH3(溶液显碱性),再通入足量的CO2的原因是( )
| A、使CO2更易被吸收 | B、NH3比CO2更易制取 | C、CO2的密度比NH3大 | D、为了增大NaHCO3的溶解度 |
侯氏制碱法的主要反应之一为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,下面对该反应涉及的有关知识发表的部分见解.其中不正确的是( )
| A、此反应可以获得固态氮肥 | B、NH3中氮元素的化合价为-3价 | C、该条件下NaHCO3的溶解度较大 | D、生成的NaHCO3不是纯碱 |
我国化学家侯德榜的“联合制碱法”工艺简洁效率高.其主要反应如下:
①NH3+H2O+CO2═NH4HCO3 ②NaCl(饱和)+NH4HCO3═NH4Cl+NaHCO3↓③2NaHCO3
Na2CO3+H2O+CO2↑下列说法不正确的是( )
①NH3+H2O+CO2═NH4HCO3 ②NaCl(饱和)+NH4HCO3═NH4Cl+NaHCO3↓③2NaHCO3
| ||
| A、①反应是化合反应,②反应是置换反应 |
| B、③反应过程中碳元素的化合价没发生改变 |
| C、③反应后的H2O和CO2可以被循环使用 |
| D、反应结束后,只得到一种产物Na2CO3 |
“NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl”是著名的“侯氏制碱法”的重要反应,反应生成的(一种盐)达到一定浓度时会从溶液中先结晶出来,下面是4位同学对该反应涉及的有关知识发表的部分见解,其中正确的是( )
| A、这个反应属于复分解反应 | B、NaHCO3一定是难溶于水的物质 | C、反应后的溶液中存在NH4+ | D、结晶出NaHCO3后的溶液中没有Na+ |
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3(析出),促进了世界制碱技术的发展.下列说法正确的是( )


| A、沉淀池中得到的沉淀是NaHCO3,因为该条件下NaHCO3的溶解度比NH4Cl小 | B、过滤得到的“母液”中一定只含有两种溶质 | C、图中X可能是氨气 | D、通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |