0 104896 104904 104910 104914 104920 104922 104926 104932 104934 104940 104946 104950 104952 104956 104962 104964 104970 104974 104976 104980 104982 104986 104988 104990 104991 104992 104994 104995 104996 104998 105000 105004 105006 105010 105012 105016 105022 105024 105030 105034 105036 105040 105046 105052 105054 105060 105064 105066 105072 105076 105082 105090 211419




 作为北京奥运会火炬使用的燃料,其燃烧后的产物是什么?某校环保小组的同学在老师的指导下选择了如下装置(铁架台等装置已略去),对丙烷在氧气中燃烧后的气体进行了检测:
作为北京奥运会火炬使用的燃料,其燃烧后的产物是什么?某校环保小组的同学在老师的指导下选择了如下装置(铁架台等装置已略去),对丙烷在氧气中燃烧后的气体进行了检测:

 和
和 .
.
 的质量分数,将其敲碎,取12.5g样品放入试管中,然后加入一定量10%的稀盐酸(杂质不与盐酸反应也不溶于水),恰好完全反应,收集到4.4g的气体.求:
的质量分数,将其敲碎,取12.5g样品放入试管中,然后加入一定量10%的稀盐酸(杂质不与盐酸反应也不溶于水),恰好完全反应,收集到4.4g的气体.求:
 的质量分数;
的质量分数;
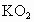 )的作用原理为:
)的作用原理为: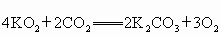
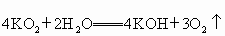 ),测定反应前后装置A的总质量,他们进行了三次实验.
),测定反应前后装置A的总质量,他们进行了三次实验.


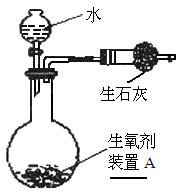
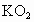 的质量分数;
的质量分数;
 样品(杂质不溶于水),取12.5克样品放入烧杯中,然后加入39.6克水使其充分溶解,静置后滤去杂质.取10克滤液,加入100克硝酸银溶液,恰好完全反应生成白色沉淀,过滤后得到107.13克的溶液,试计算:(计算结果精确到0.1%)
样品(杂质不溶于水),取12.5克样品放入烧杯中,然后加入39.6克水使其充分溶解,静置后滤去杂质.取10克滤液,加入100克硝酸银溶液,恰好完全反应生成白色沉淀,过滤后得到107.13克的溶液,试计算:(计算结果精确到0.1%)

 和
和 完全转化为
完全转化为 沉淀,需要20%NaOH溶液多少克?
沉淀,需要20%NaOH溶液多少克?
 ,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0g/L)?
,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0g/L)? 溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:
溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:
 溶液呈______________性;
溶液呈______________性;


