题目内容
3.结合图示实验装置,回答下列问题.
(1)图中a、b仪器的名称:a酒精灯,b长颈漏斗.
(2)用高锰酸钾固体制氧气,选用的发生装置是A(填“A”、“B”或“C”),装入药品前应先检查装置的气密性,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用B装置制取二氧化碳时,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.b中应加入石灰石或大理石.要获得干燥的二氧化碳,除发生装置外,还应选用盛放浓硫酸的D装置.如用E装置收集CO2,则气体应从c端通入(填“c”或“d”).
(4)用块状固体和液体不加热制取气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是可以控制反应的发生和停止或节约药品(答出一点即可).
分析 酒精灯是常用的加热仪器,长颈漏斗方便加液体药品;装入药品前应先:检查装置的气密性;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳可以用浓硫酸干燥.如用E装置收集CO2,则气体应从长管进入,因为二氧化碳的密度比空气的密度大;C装置代替B装置的优点是:可以控制反应的发生和停止、节约药品等.
解答 解:(1)酒精灯是常用的加热仪器,长颈漏斗方便加液体药品;故答案为:酒精灯;长颈漏斗;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;装入药品前应先:检查装置的气密性;故答案为:A;检查装置的气密性;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;b中应加入石灰石或大理石,二氧化碳可以用浓硫酸干燥;如用E装置收集CO2,则气体应从长管进入,因为二氧化碳的密度比空气的密度大;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;石灰石或大理石;c;
(4)C装置代替B装置的优点是:可以控制反应的发生和停止、节约药品等,故答案为:可以控制反应的发生和停止或节约药品;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、检查装置的气密性和装置的改进等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| A. | Mg | B. | Zn | C. | Ag | D. | Cu |
| A. | 原子是微小的实心球体,可以再分 | |
| B. | 单个SO2分子有刺激性气味 | |
| C. | 纯净的氢气在氧气中完全燃烧后,生成的物质是由同一种粒子构成的 | |
| D. | 离子是原子失去电子后生成的粒子 |
| $\stackrel{+1}{H}$ | $\stackrel{+1}{Na}$ | $\stackrel{+2}{Ca}$ | $\stackrel{+2}{Mg}$ | $\stackrel{+2}{Fe}$ | $\stackrel{+3}{Fe}$ | |
| $\stackrel{-1}{Cl}$ | ||||||
| $\stackrel{-2}{O}$ | ||||||
| $\stackrel{-1}{N{O}_{3}}$ | ||||||
| $\stackrel{-2}{S{O}_{4}}$ |
| A. | 溶液质量减小 | B. | 溶液仍为t℃时的饱和溶液 | ||
| C. | 溶质在t℃时的溶解度不变 | D. | 溶质质量分数减小 |
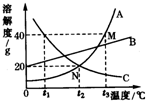 如图是A、B、C三种固体物质的溶解度曲线,从图中你能获得哪些信息(写三条)
如图是A、B、C三种固体物质的溶解度曲线,从图中你能获得哪些信息(写三条)