题目内容
18.化学是以实验为基础的学科.根据图1、图2、图3回答下列问题:
(1)图1是测定空气中氧气含量的实验,实验后发现测定空气中氧气含量偏低,原因可能是装置气密性不好或红磷的量不足或没有冷却到室温就打开弹簧夹(填一种即可).
(2)图2是细铁丝在氧气中燃烧的实验,集气瓶中未预先装少量的水或铺一层细沙,可能引起的后果是生成的高温熔融物炸裂瓶底.
(3)图3是验证化学反应前后质量守恒的实验,反应结束后天平的指针偏右,该反应是否遵守质量守恒定律是(填“是”或“否”).造成指针偏右的原因原因是生成的二氧化碳逸散到空气中使质量减小,故指针偏右.
分析 (1)根据测定空气中氧气含量实验的注意事项进行解答;铁丝在氧气中燃烧时放出大量的热,能够产生高温的熔化物,如果直接落在集气瓶中会引起集气瓶的炸裂;
(3)根据质量守恒定律的适用范围来分析,根据盐酸与碳酸钠反应生成了二氧化碳气体,逸散到了空气中会使烧杯中物质的质量减少来分析解答.
解答 解:(1)实验后发现测定空气中氧气含量偏低,造成这种结果的可能原因是装置气密性不好、红磷的量不足或没有冷却到室温就打开弹簧夹.故填:装置气密性不好或红磷的量不足或没有冷却到室温就打开弹簧夹;
(2)铁丝在盛有氧气的集气瓶中剧烈燃烧,火星四射,放出大量的热,生成黑色固体.防止生成的熔融物炸裂瓶底,在瓶底铺一层细沙或盛少量水,集气瓶中未预先装少量的水或铺一层细沙,可能引起的后果是生成的高温熔融物炸裂瓶底,故填:生成的高温熔融物炸裂瓶底;
(3)所有的化学变化都遵循质量守恒定律.盐酸与碳酸钠反应生成氯化钠、水、二氧化碳,而烧杯是敞开的,所以生成的二氧化碳逸散到空气中使质量减小,故指针偏右,但这并不意味着该反应不遵循质量守恒定律;
故填:是;生成的二氧化碳逸散到空气中使质量减小,故指针偏右.
点评 此题以图示的形式综合考查了正确判断实验现象及规范进行基本的实验操作的综合题,解题时应充分利用题中给予的信息,进行筛选分析,得出正确答案.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
8.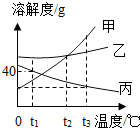 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质质量相等 | |
| B. | 甲和乙的溶解度都随温度的升高而增大 | |
| C. | 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙 | |
| D. | t1℃时,甲、丙的饱和溶液中溶质的质量分数为40% |
9.甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了下图所示的四组实验方案.
(1)其中能达到实验目的是C、D.
(2)在C组实验中发生的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有CaCO3物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和NaOH三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
(6)乙同学认为甲同学第②步验证的结论不严密,原因是氢氧化钠溶液也显碱性,还可能是氢氧化钠或氢氧化钠和氢氧化钙的混合物.

(1)其中能达到实验目的是C、D.
(2)在C组实验中发生的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有CaCO3物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和NaOH三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
| 实验内容 | 预测现象 | 结论 |
| 取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
| ②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
| ③若有白色沉淀,溶液呈红色 | 物质是碳酸钠和氢氧化钠的混合物 |
6.下列物质的性质与用途不对应的是( )
| A. | 汽油具有可燃性--用作燃料 | B. | 氧气难溶于水--用于急救病人 | ||
| C. | 干冰容易升华吸热--用于人工降雨 | D. | 氮气不活泼--用于食品防腐 |
13.化学概念之间具有如下图所示的并列、包含、交叉等关系,对下列概念间的关系说法正确的是( )

| A. | 化合物与酸、碱、盐属于并列关系 | B. | 纯净物与混合物属于包含关系 | ||
| C. | 单质与化合物属于交叉关系 | D. | 氧化反应与化合反应属于交叉关系 |
3.小明同学将一定量的氢化钙(CaH2)加入到足量的Na2CO3溶液中,充分反应后过滤,分离出滤渣和滤液.
【提出问题】滤液中溶质的成份是什么?
【查阅资料】CaH2遇水迅速反应生成Ca(OH)2和H2.反应的化学方程式为CaH2+2H2O═Ca(OH)2+2H2↑.
【结论推理】滤液中溶质一定有NaOH,可能有Na2CO3或Ca(OH)2.
【实验验证】请结合题意,在下列表格的空白中填写恰当的内容.
【反思与拓展】
(1)如果要从上述滤液中以最小生产成本获得大量NaOH,你建议向滤液中加入适量的氢氧化钙溶液.
(2)小明同学认为CaH2与水的反应是复分解反应.请谈谈你的看法并说明理由不属于复分解反应;氢化钙和水反应生成氢氧化钙和氢气,生成物中氢气属于单质.
【提出问题】滤液中溶质的成份是什么?
【查阅资料】CaH2遇水迅速反应生成Ca(OH)2和H2.反应的化学方程式为CaH2+2H2O═Ca(OH)2+2H2↑.
【结论推理】滤液中溶质一定有NaOH,可能有Na2CO3或Ca(OH)2.
【实验验证】请结合题意,在下列表格的空白中填写恰当的内容.
| 实验方法 | 实验现象 | 实验结论 |
| 取滤液少许,向其中滴加 Na2CO3溶液. | 无明显显现 | (1)说明滤液中没有氢氧化钙 |
| (2)另取滤液,向其中加入足量稀盐酸. | 有气体放出 | 滤液中有Na2CO3存在 |
(1)如果要从上述滤液中以最小生产成本获得大量NaOH,你建议向滤液中加入适量的氢氧化钙溶液.
(2)小明同学认为CaH2与水的反应是复分解反应.请谈谈你的看法并说明理由不属于复分解反应;氢化钙和水反应生成氢氧化钙和氢气,生成物中氢气属于单质.
8.维生素C(C6H8O6)主要存在于蔬菜和水果中,补充一定量的维生素有利于身体的健康,下面的说法正确的是( )
| A. | 维生素C是一种氧化物 | |
| B. | 维生素C中碳、氢、氧元素的质量比为3:4:3 | |
| C. | 一个维生素C的分子中共含有20个原子 | |
| D. | 维生素C中碳元素的质量分数最大 |
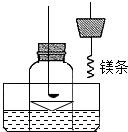 某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,设计了如下方案进行验证.
某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,设计了如下方案进行验证.