题目内容
18.臭氧(O3)能吸收大部分紫外线,保护地球生物,臭氧属于( )| A. | 纯净物 | B. | 混合物 | C. | 氧气 | D. | 氧化物 |
分析 理解纯净物、混合物以及氧化物的含义既能解此题.
解答 解:由臭氧(O3)的化学式知道,臭氧由一种物质组成,属于纯净物,且臭氧是由一种元素组成的,属于单质,臭氧与氧气的化学式不同,属于不同物质.
故选A.
点评 此题考查纯净物、混合物及氧化物的含义,理解这些含义既解此题.

练习册系列答案
相关题目
8.以下两幅微观示意图揭示了化学变化的微观实质.相关说法中正确的是( )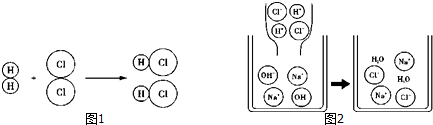

| A. | 图1说明了化学变化前后分子数一定不变 | |
| B. | 原子在化学变化中是可以再分的 | |
| C. | 两幅图表示的都是化合反应 | |
| D. | 图2中H+发生化学变化而Na+没有 |
3.小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体开展探究,请你与他们一起进行探究.
提出问题:
这瓶氢氧化钠固体是否变质?
猜想与假设:
氢氧化钠没有变质;该氢氧化钠部分变质;该氢氧化钠全部变质
设计实验:
取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
反思与交流:
(4)久置的氢氧化钠变质的原因是(用化学方程式)CO2+2NaOH=Na2CO3+H2O.
探究与拓展:
(5)为进一步探究氢氧化钠的变质程度,小明称取20克氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产上气泡为止,共消耗稀盐酸100克,反应后称的烧杯中溶液的质量为115.6克,求该样品中碳酸钠的质量分数(要写出计算过程).
提出问题:
这瓶氢氧化钠固体是否变质?
猜想与假设:
氢氧化钠没有变质;该氢氧化钠部分变质;该氢氧化钠全部变质
设计实验:
取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A 于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想(1)不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式)CO2+2NaOH=Na2CO3+H2O.
探究与拓展:
(5)为进一步探究氢氧化钠的变质程度,小明称取20克氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产上气泡为止,共消耗稀盐酸100克,反应后称的烧杯中溶液的质量为115.6克,求该样品中碳酸钠的质量分数(要写出计算过程).
10.空气中化学性质最活泼的气体是( )
| A. | N2 | B. | CO2 | C. | O2 | D. | 稀有气体 |
8.常见的净化水方法有:①过滤、②用木炭吸附、③煮沸、④用药杀菌消毒.现要将黄色浑浊的河水净化成生活饮用水,应选用的方法和顺序为( )
| A. | ①②③④ | B. | ④①③② | C. | ③①④② | D. | ①②④③ |
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: