题目内容
8.以下两幅微观示意图揭示了化学变化的微观实质.相关说法中正确的是( )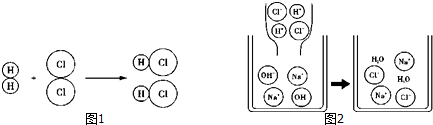
| A. | 图1说明了化学变化前后分子数一定不变 | |
| B. | 原子在化学变化中是可以再分的 | |
| C. | 两幅图表示的都是化合反应 | |
| D. | 图2中H+发生化学变化而Na+没有 |
分析 根据两幅微观示意图,前一幅图所表示的反应为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,后一幅图所表示的反应为NaOH+HCl═NaCl+H2O.根据微粒的变化,分析分子、原子的变化,根据反应的特点分析判断反应的类型.
解答 解:由两幅微观示意图可知,前一幅图所表示的反应为:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,后一幅图所表示的反应为:NaOH+HCl═NaCl+H2O.
A、图1说明了化学变化前后分子数不变,但不能说明在所有的化学变化中分子数目不变.故A错误;
B、由微粒的变化可知,分子在化学变化中可以再分,原子在化学变化中是不能再分的,而是重新组合.故B错误;
C、由方程式可知,第一幅图示表示的反应是化合反应,第二幅图示表示的反应是复分解反应,故C错误;
D、第二幅图示表示氢离子和氢氧根离子结合成水分子,而钠离子和氯离子没有参加反应,故D正确.
故选D.
点评 本题根据微观示意图考查了化学反应的实质,完成此题,可以依据已有的知识结合图示进行.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
13.电镀厂的废水中含有H2SO4和CuSO4,为了回收Cu(OH)2并得到化肥,工厂化验室取来200g废水,逐滴加入KOH溶液,反应情况如图1所示.请回答:
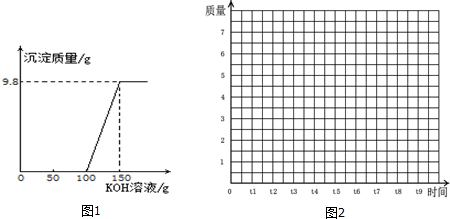
(1)求所用的KOH溶液的溶质质量分数;
(2)若每天处理200吨废水,可制得多少吨K2SO4.
(3)某化学兴趣小组的同学将8gFe2O3在高温下不断通入CO,测得生成CO2的质量与反应时间的变化关系如表所示:
①上表中有一组数据不科学,请指出并加以修正.
②请在图2中画出生成CO2的质量与反应时间的关系.

(1)求所用的KOH溶液的溶质质量分数;
(2)若每天处理200吨废水,可制得多少吨K2SO4.
(3)某化学兴趣小组的同学将8gFe2O3在高温下不断通入CO,测得生成CO2的质量与反应时间的变化关系如表所示:
| 反应 时间 | t0 | t1 | t2 | t3 | t4 | t5 | t6 | t7 | t8 | t9 |
| CO2 质量/g | 0 | 2.5 | 4 | 4.8 | 5.5 | 7.0 | 6.3 | 6.5 | 6.6 | 6.6 |
②请在图2中画出生成CO2的质量与反应时间的关系.
20.下列有关实验室的试剂保存方法,请你说明原因.
| 选项 | 保存方法 | 原因 |
| A | 白磷应保存在冷水中 | 白磷的着火点低 |
| B | 浓硫酸应密封保存 | 浓硫酸具有吸水性 |
| C | 氢氧化钠应密封保存 | 氢氧化钠固体在空气中易潮解并能与二氧化碳反应生成碳酸钠和水 |
17.粗盐是含有MgCl2、CaCl2、Na2SO4的食盐,某兴趣小组把粗盐进行提纯,并制备NaHCO3晶体,其设计流程如下:
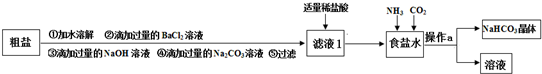
下列说法正确的是( )

下列说法正确的是( )
| A. | 滴加过量Na2CO3溶液只是为了除去粗盐中的Ca2+ | |
| B. | 滤液1中加适量盐酸发生的反应只有1个 | |
| C. | 在食盐水中通NH3、CO2发生反应的化学方程式是NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl | |
| D. | 操作a用到的玻璃仪器只有烧杯 |
18.臭氧(O3)能吸收大部分紫外线,保护地球生物,臭氧属于( )
| A. | 纯净物 | B. | 混合物 | C. | 氧气 | D. | 氧化物 |
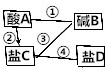 酸、碱、盐之间是可以相互转化,如图所示,A、B、C、D是初中化学常见的物质;常见气体a可以转化为A,其中一种盐的俗称是纯碱.图中“-”表示两端的物质间能发生化学反应且生成沉淀,“→”表示两端的物质间存在转化关系.
酸、碱、盐之间是可以相互转化,如图所示,A、B、C、D是初中化学常见的物质;常见气体a可以转化为A,其中一种盐的俗称是纯碱.图中“-”表示两端的物质间能发生化学反应且生成沉淀,“→”表示两端的物质间存在转化关系.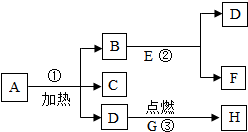 A.B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.试推断:
A.B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.试推断: