题目内容
为保证驾乘人员人身安全,许多汽车中增设了安全气囊,内置叠氮化钠(NaN3),在汽车发生一定强度的碰撞时,叠氮化钠发生分解反应:2NaN3→2Na+3N2↑,立即气体充满气囊,以达到保护驾乘人员的目的.
若填充一安全气囊需要0.9mol氮气,则约含 个氮原子,需要有 mol的叠氮化钠发生上述的分解反应,这些叠氮化钠的质量是 g.
若填充一安全气囊需要0.9mol氮气,则约含
考点:有关化学式的计算和推断
专题:化学式的计算
分析:先求出N2的物质量,再根据阿伏加德罗常数求出原子的总个数.
根据化学方程式,求叠氮化钠(NaN3)的物质的量,根据其摩尔质量,求其质量.
根据化学方程式,求叠氮化钠(NaN3)的物质的量,根据其摩尔质量,求其质量.
解答:解:已知氮化钠的摩尔质量M=65g/mol,阿伏加德罗常数NA=6.02×1023mol-1.汽车的安全气囊在汽车发生一定强度的碰撞时,利用叠氮化钠(NaN3)固体发生分解反应,迅速产生氮气和固态钠,反应的化学方程式为:2NaN3
2Na+3N2↑.
故可求填充一安全气囊需要0.9mol氮气,则约含氮原子的个数为:0.9mol×6.02×1023mol-1×2=1.0836×1024;需要叠氮化钠的物质的量为:0.9mol×
=0.6mol,则其质量为0.6mol×65g/mol=39g.
故答案为:1.0836×1024;0.6;39
| 撞击 |
. |
故可求填充一安全气囊需要0.9mol氮气,则约含氮原子的个数为:0.9mol×6.02×1023mol-1×2=1.0836×1024;需要叠氮化钠的物质的量为:0.9mol×
| 2 |
| 3 |
故答案为:1.0836×1024;0.6;39
点评:加强对基本概念的记忆,基本方法的学习利用,是学好3-3的基本方法.此处要求不高,不用做太难的题目.

练习册系列答案
相关题目
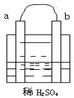 在图所示的装置中,a的活动性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是.( )
在图所示的装置中,a的活动性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是.( )| A、碳棒上有气体放出,溶液的pH增大 |
| B、a是正极,b是负极 |
| C、导线中有电子流动,电子从a极流到b极 |
| D、a极上发生了氧化反应 |
我们生活在物质的世界里,物质在不断地变化.下列自然现象,属于化学变化的是( )
| A、衣服晾干 | B、玻璃杯摔碎 |
| C、天然气燃烧 | D、酒精挥发 |
化学反应前后,肯定没有变化的是( )
①原子的数目;②元素的种类;③分子的数目;④分子的种类;⑤原子的质量;⑥物质的总质量;⑦物质的种类;⑧原子的种类;⑨物质的状态.
①原子的数目;②元素的种类;③分子的数目;④分子的种类;⑤原子的质量;⑥物质的总质量;⑦物质的种类;⑧原子的种类;⑨物质的状态.
| A、①③⑤⑥⑨ | B、②④⑦⑧⑨ |
| C、①②③⑤ | D、①②⑤⑥⑧ |
 如图,将几块经过烘烤并放冷的木炭(或活性炭),投到盛满某种(相对分子质量≥20)有色气体的集气瓶中,并轻轻摇动.你能观察到的现象是
如图,将几块经过烘烤并放冷的木炭(或活性炭),投到盛满某种(相对分子质量≥20)有色气体的集气瓶中,并轻轻摇动.你能观察到的现象是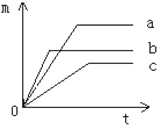 质量相等的三种不同金属与足量的稀硫酸反应,都生成+2价的化合物,其反应情况如图所示(图中t表示反应的时间,m表示产生氢气的质量).回答:
质量相等的三种不同金属与足量的稀硫酸反应,都生成+2价的化合物,其反应情况如图所示(图中t表示反应的时间,m表示产生氢气的质量).回答: