题目内容
化学与生活密切相关.
(1)人体可以从水果和蔬菜中摄取 ,该类物质需要量很小,但可以起到调节新陈代谢、预防疾病和维持身体健康的作用.
(2)如营养成分表是某儿童补铁药品的部分说明.说明中的“铁”指的是 (填“单质”、“元素”或“分子”).
(3)某些食品的近似pH如表:
其中酸性最强的是 ,胃酸过多的人应食用 .
(4)在催化剂作用下,乙醇与氧气、氢氧化钠在燃料电池中反应生成碳酸钠和另一种物质,并得到电能,请完成该反应的化学方程式:CH3CH2OH+3O2+4NaOH
2Na2CO3+ .
(1)人体可以从水果和蔬菜中摄取
(2)如营养成分表是某儿童补铁药品的部分说明.说明中的“铁”指的是
| 营养成分 | 每片含量 | 每100g含量 |
| 铁 | 6.7mg | 1.12g |
| 叶酸 | 255pg | 42.5mg |
| 食品 | 柠檬汁 | 苹果汁 | 葡萄汁 | 番茄汁 | 牛奶 | 玉米粥 |
| pH | 2.4 | 3.1 | 4.2 | 4.4 | 6.5 | 7.8 |
(4)在催化剂作用下,乙醇与氧气、氢氧化钠在燃料电池中反应生成碳酸钠和另一种物质,并得到电能,请完成该反应的化学方程式:CH3CH2OH+3O2+4NaOH
| 催化剂 |
考点:生命活动与六大营养素,溶液的酸碱性与pH值的关系,元素的概念,质量守恒定律及其应用
专题:化学用语和质量守恒定律,化学与生活
分析:(1)根据水果和蔬菜中富含的营养素来分析;
(2)根据元素与构成对物质的微粒的关系来分析;
(3)根据溶液的pH与酸碱性的关系以及酸碱中和的原理来分析;
(4)根据质量守恒定律的微观原因来分析.
(2)根据元素与构成对物质的微粒的关系来分析;
(3)根据溶液的pH与酸碱性的关系以及酸碱中和的原理来分析;
(4)根据质量守恒定律的微观原因来分析.
解答:解:(1)水果和蔬菜中富含维生素;故填:维生素;
(2)物质是由元素组成的,故在此“铁”既不是指的单质,也不是指的分子,而是指元素;故填:元素;
(3)pH越小,酸性越强,由图表可知柠檬汁的pH最小,故它的酸性最强;胃酸过多的病人应该多食用显碱性的食物,也就是pH大于7的食物,如玉米粥;故填:柠檬汁;玉米粥;
(4)根据化学反应前后,原子的种类、数目均不改变可知,
反应前 反应后
C 2 2
H 10 0
O 11 6
Na 4 4
故生成物中还应该含有10个氢原子和5个氧原子,故填写:5H2O.
(2)物质是由元素组成的,故在此“铁”既不是指的单质,也不是指的分子,而是指元素;故填:元素;
(3)pH越小,酸性越强,由图表可知柠檬汁的pH最小,故它的酸性最强;胃酸过多的病人应该多食用显碱性的食物,也就是pH大于7的食物,如玉米粥;故填:柠檬汁;玉米粥;
(4)根据化学反应前后,原子的种类、数目均不改变可知,
反应前 反应后
C 2 2
H 10 0
O 11 6
Na 4 4
故生成物中还应该含有10个氢原子和5个氧原子,故填写:5H2O.
点评:化学知识源于生活,又服务于生活,化学知识也涉及到我们的日常生活.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
铜与浓硫酸共热的条件下可以发生化学反应:Cu+2H2SO4=CuSO4+SO2↑+2H2O,但是在工业生产硫酸铜的流程是:①2Cu+O2=2CuO②CuO+H2SO4=CuSO4+H2O,你认为这样的优点是( )
| A、节约能源 |
| B、不产生污染大气的二氧化硫 |
| C、提高硫酸的利用率 |
| D、提高铜的利用率 |
下列物质的分类,对应正确的是( )
| A、混合物:水银、天然气 |
| B、新能源:太阳能、潮汐能 |
| C、合成材料:合金、塑料 |
| D、碳单质:金刚石、石灰石 |
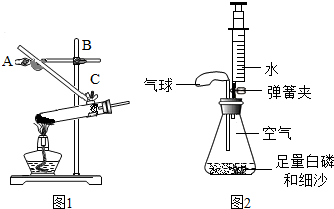 实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神.
实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神.