题目内容
铜与浓硫酸共热的条件下可以发生化学反应:Cu+2H2SO4=CuSO4+SO2↑+2H2O,但是在工业生产硫酸铜的流程是:①2Cu+O2=2CuO②CuO+H2SO4=CuSO4+H2O,你认为这样的优点是( )
| A、节约能源 |
| B、不产生污染大气的二氧化硫 |
| C、提高硫酸的利用率 |
| D、提高铜的利用率 |
考点:物质的相互转化和制备,金属的化学性质,酸的化学性质
专题:物质的制备
分析:由于浓硫酸与铜直接反应时会生成有毒的二氧化硫,且需要的硫酸量较大所以一般不采用这种方式进行.
解答:解:在浓硫酸与铜的反应中不但生成了污染物二氧化硫,而且还消耗了较多的硫酸,因为硫以二氧化硫的形式跑掉了一部分,而利用将铜屑在空气中加热氧化,然后浸入稀硫酸中反应过滤,并反复加热和浸入操作,有效地避免了这一些.
故选BC
故选BC
点评:此题是对硫酸铜制取的考查,解题的关键是分析不同方式在环保及节约两个方面的不同.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
下列化学用语表达不正确的是( )
| A、2C1--两个氯原子 |
| B、S2---负二价的硫元素 |
| C、2Fe2+--两个亚铁离子 |
| D、O2--氧气或一个氧分子 |
下列操作所用试剂不正确的是( )
| A、干燥氨气-碱石灰 |
| B、干燥CO气体-浓硫酸 |
| C、洗去附着在试管内壁的氯化银-稀硝酸 |
| D、洗去附着在试管内壁的氢氧化铜-稀硫酸 |
下列厨房中常见的操作或现象,其中涉及化学变化的是( )
| A、水果榨汁 | B、萝卜剁碎 |
| C、铁锅生锈 | D、汤中加盐 |
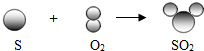
 A-Z都是初中化学的常见物质,其中A是发酵粉的一种主要原料,俗称小苏打,B是胃酸的主要成分,C和M的组成元素相同,常温下E是液体,Y、Z是黑色固体,N是红色粉末,G是一种碱,农业上常用作改良酸性土壤.它们之间有如图反应关系:
A-Z都是初中化学的常见物质,其中A是发酵粉的一种主要原料,俗称小苏打,B是胃酸的主要成分,C和M的组成元素相同,常温下E是液体,Y、Z是黑色固体,N是红色粉末,G是一种碱,农业上常用作改良酸性土壤.它们之间有如图反应关系: