题目内容
20.对下列反应的化学方程式的书写及反应类型的判断都正确的是( )| 选项 | 化学反应方程式 | 反应类型 |
| A红磷在空气中燃烧 | 4P+5O2═2P2O5 | 氧化反应 |
| B氧化铜放入稀盐酸中 | CuO+2HCl═CuCl+H2O | 复分解反应 |
| C煤炉上方产生淡蓝色火焰 | 2CO2+C$\frac{\underline{\;点燃\;}}{\;}$2CO | 化合反应 |
| D过氧化氢分解制氧气 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | 分解反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确;若化学方程式书写正确,再判断反应类型是否正确.
解答 解:A、该化学方程式缺少反应条件,正确的化学方程式应为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,故选项错误.
B、该化学方程式氯化铜的化学式书写错误,正确的化学方程式应为:CuO+2HCl═CuCl2+H2O,故选项错误.
C、煤炉上方产生淡蓝色火焰,是因为一氧化碳燃烧生成二氧化碳,正确的化学方程式应为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;故选项错误.
D、该化学方程式书写完全正确,且该反应符合“一变多”的特征,属于分解反应,故选项正确.
故选:D.
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

练习册系列答案
相关题目
11.甲、乙、丙三个实验小组围绕“酸碱中和反应”在老师引导下开展探究活动,请你参与学习并帮助填写空格.
【查阅资料】Na2SO4溶液呈中性
【演示实验】将一定量的稀H2SO4加入到盛有无色酚酞试液和NaOH溶液的小烧杯中.当看到溶液由红色变为无色现象,证明稀硫酸和氢氧化钠发生了化学反应.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】部分同学产生了疑问:反应后溶液中溶质除了酚酞,还有什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出实验方案中有一个是错误的,错误的原因是氯化钡能与硫酸钠反应产生白色沉淀.
【反思拓展】(1)在分析反应后所得物质的成分时,除了考虑生成物,还应该考虑反应物是否过量.
(2)根据所学的化学知识,你还有哪些方法证明所得的溶液中含有硫酸,请列举一种方法中使用试剂的名称锌(合理均可).
【查阅资料】Na2SO4溶液呈中性
【演示实验】将一定量的稀H2SO4加入到盛有无色酚酞试液和NaOH溶液的小烧杯中.当看到溶液由红色变为无色现象,证明稀硫酸和氢氧化钠发生了化学反应.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】部分同学产生了疑问:反应后溶液中溶质除了酚酞,还有什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出实验方案中有一个是错误的,错误的原因是氯化钡能与硫酸钠反应产生白色沉淀.
【反思拓展】(1)在分析反应后所得物质的成分时,除了考虑生成物,还应该考虑反应物是否过量.
(2)根据所学的化学知识,你还有哪些方法证明所得的溶液中含有硫酸,请列举一种方法中使用试剂的名称锌(合理均可).
15. 如图所示实验台上有一瓶标签残缺的试剂,同学们对此进行了如下探究:
如图所示实验台上有一瓶标签残缺的试剂,同学们对此进行了如下探究:
【提出问题】这瓶溶液是什么?
【假设猜想】(1)针对疑问,大家纷纷提出猜想.同学们的猜想如下:
甲同学猜想:Na2SO4溶液
乙同学猜想:NaOH溶液
丙同学猜想:Na2CO3溶液
请写出你的猜想是NaCl(任写一种)
【查阅资料】硫酸钠溶液,氯化钠溶液等呈中性,碳酸钠溶液呈碱性.
【实验探究】(2)同学们为了验证自己的猜想,利用试剂瓶中的溶液,并选用老师提供的pH试纸,无色酚酞溶液,BaCl2溶液等,进行如下三个方案的探究.请你帮助他们完成表格:
【得出结论】通过实验探究,同学们一致确定每位学生猜想都不合理.
【评价反思】(3)请你帮甲同学分析猜想不合理的原因氯化钠也显中性,pH等于7.
(4)你能否帮丙同学设计一个实验验证他的猜想继续向沉淀中加入硝酸沉淀溶解,或者直接向原溶液加入稀盐酸,有气泡生成.
 如图所示实验台上有一瓶标签残缺的试剂,同学们对此进行了如下探究:
如图所示实验台上有一瓶标签残缺的试剂,同学们对此进行了如下探究:【提出问题】这瓶溶液是什么?
【假设猜想】(1)针对疑问,大家纷纷提出猜想.同学们的猜想如下:
甲同学猜想:Na2SO4溶液
乙同学猜想:NaOH溶液
丙同学猜想:Na2CO3溶液
请写出你的猜想是NaCl(任写一种)
【查阅资料】硫酸钠溶液,氯化钠溶液等呈中性,碳酸钠溶液呈碱性.
【实验探究】(2)同学们为了验证自己的猜想,利用试剂瓶中的溶液,并选用老师提供的pH试纸,无色酚酞溶液,BaCl2溶液等,进行如下三个方案的探究.请你帮助他们完成表格:
| 甲同学 | 乙同学 | 丙同学 | |
| 实验方案 | 测溶液pH | 滴加无色酚酞溶液 | 滴加BaCl2溶液 |
| 实验操作 | 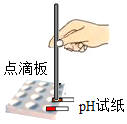 | 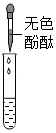 | 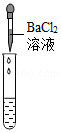 |
| 实验现象 | 试纸不变色,对比标准的比色卡,pH=7 | 溶液变红 | 产生白色沉淀 |
| 实验方程式 | Na2CO3+BaCl2=BaCO3↓+2NaCl | ||
| 实验结论 | 甲同学猜想成立 | 乙同学猜想成立 | 丙同学猜想成立 |
【评价反思】(3)请你帮甲同学分析猜想不合理的原因氯化钠也显中性,pH等于7.
(4)你能否帮丙同学设计一个实验验证他的猜想继续向沉淀中加入硝酸沉淀溶解,或者直接向原溶液加入稀盐酸,有气泡生成.
 干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质$?_{反映}^{决定}$物质用途”这一角度分析干冰具有的性质和用途.
干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质$?_{反映}^{决定}$物质用途”这一角度分析干冰具有的性质和用途. 某班化学课外活动小组的同学设计了一套能验证一氧化碳性质并带有趣味性的实验,效果明显.实验装置如下图所示:当打开开关a(同时在尖嘴处放一火源),通入适量的一氧化碳后,关闭开关a和b,并撤掉火源约10~15min后,可观察到A中鱼仍然活着,B中蛙死亡,C中正常的深红色血液变成鲜红色.然后打开开关b,同时再在尖嘴导管处点燃.试回答:
某班化学课外活动小组的同学设计了一套能验证一氧化碳性质并带有趣味性的实验,效果明显.实验装置如下图所示:当打开开关a(同时在尖嘴处放一火源),通入适量的一氧化碳后,关闭开关a和b,并撤掉火源约10~15min后,可观察到A中鱼仍然活着,B中蛙死亡,C中正常的深红色血液变成鲜红色.然后打开开关b,同时再在尖嘴导管处点燃.试回答: