题目内容
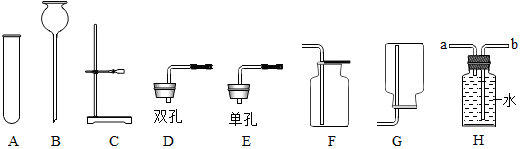
20.下列实验设计合理的是( ) |  |  |  |
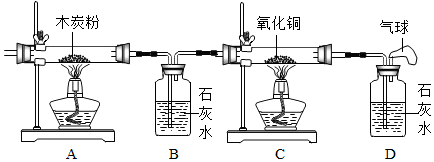
| A.验证氢气的密度比空气小 | B.验证铁生锈的条件 | C.探究呼出气体与空气中氧气含量不同 | D.用木炭测定空气中氧气含量 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据吹出的肥皂泡上升,进行分析判断.
B、根据铁锈蚀的条件,进行分析判断.
C、根据氧气能支持燃烧,进行分析判断.
D、所选除氧剂要具备以下特征:本身能够在空气中燃烧;本身的状态为非气体;生成的物质为非气态.
解答 解:A、用氢气吹肥皂泡,吹出的肥皂泡上升,说明氢气的密度比空气小,故选项实验设计合理.
B、通过对比三支试管中铁锈蚀的现象,第一支试管中的铁钉生锈,第二支、第三支试管中的铁钉没有生锈,第一支试管中的铁钉能与氧气、水充分接触;第二支、第三支试管中的铁钉分别能与空气、水充分接触,可以验证铁生锈的条件,故选项实验设计合理.
C、氧气能支持燃烧,氧气含量越高,燃烧越旺;但带火星的木条在空气和呼出的气体中均会熄灭,不能探究呼出气体与空气中氧气含量不同,故选项实验设计不合理.
D、木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,不能用来测定空气中氧气含量;故选项实验设计不合理.
故选:AB.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
8.下列公共标志与消防安全无关的是( )


| A. | ①② | B. | ②③ | C. | ③④ | D. | ③④⑤ |
9.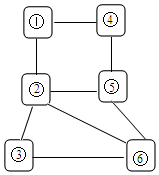 如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
 如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| A | CO2 | NaOH | HCl | Ca(OH)2 | CuCl2 | Fe |
| B | CaO | HCl | Fe | H2SO4 | Na2CO3 | Ca(OH)2 |
| C | Fe | H2SO4 | BaCl2 | Cu(NO3)2 | Ca(OH)2 | Na2CO3 |
| D | Zn | HCl | CaCO3 | CuSO4 | NaOH | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
8. 菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
说明:菱镁矿中的杂质不溶于水,不与酸发生反应.
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是9.8%.
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标中作图,并标出曲线折点的坐标)
 菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究.取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:| 加入H2SO4溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是9.8%.
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标中作图,并标出曲线折点的坐标)