题目内容
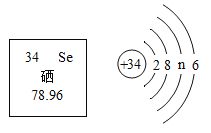
【题目】根据如图某食用盐商标上的部分文字,用化学用语填空:

(1)图中一种非金属元素的符号______________;
(2)氯化钠的化学式_________________;
(3)碘酸钾(KIO3) 中阴离子的符号______________________。
【答案】Cl (或O、I、Si) NaCl IO3-
【解析】
(1)表中的非金属元素有氯、氧、碘、硅等元素,元素符号为:Cl、O、I、Si;
(2)氯化钠是由显+1价的钠元素和显-1价的氯元素组成,根据化合价原则,其化学式为:NaCl;
(3)碘酸钾(KIO3) 中阴离子是碘酸根离子,离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,故碘酸根离子可表示为:![]() ;
;

【题目】材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁。
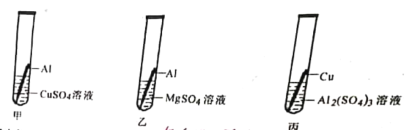
(一)单质铁钉的一系列变化。
![]()
(1)变化①的原因是铁与空气中的水、______等物质发生一系列复杂反应的结果。
(2)变化②的实验现象是:铁锈消失,______,发生反应的化学方程式为______
(二)铁及其化合物的实验
硫酸亚铁铵(俗称摩尔盐)化学式为FeSO4· (NH4)2SO4· 6H2O,是一种重要的化工原料, 用途十分广泛。
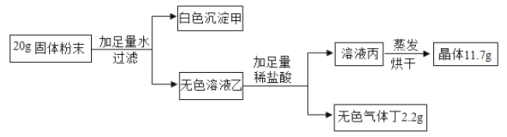
Ⅰ 硫酸亚铁铵晶体制备。 资料:溶质从溶液里结晶析出时,晶体里结合着一定数目的水分子,这样的水分子叫结晶水。 硫酸亚铁铵晶体易溶于水,不溶于乙醇。
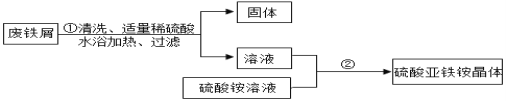
(1)在步骤①前要对废铁屑进行预处理,先利用洗涤剂的______作用除去油污。
(2)操作②中发生了一系列变化,目的是得到硫酸亚铁铵晶体。其中的操作顺序是: b→______→______→d;
a 过滤b 加热浓缩c 降温结晶d 洗涤干燥
(3)操作②中使用乙醇洗涤。这样做的优点是______;
A 避免用水洗涤所造成的晶体损耗B 酒精易挥发,可低温晾干晶体
Ⅱ 硫酸亚铁铵晶体热分解实验
兴趣小组称取此晶体样品 39.2g,在科研人员的指导下用如图装置进行热分解实验。
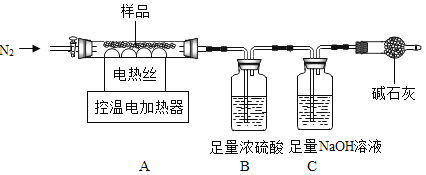
(查阅资料)①硫酸亚铁铵晶体在 200℃完全失去结晶水,剩余物在 500℃完全分解为铁的某氧化物、SO2、SO3、NH3 和 H2O。
②B 装置中浓硫酸只能吸收 NH3、SO3 和 H2O。
(1)装配好实验装置后,先要______。
(2)控制不同的温度对 A 中固体加热,测得装置 B 和 C 中的质量变化如表。
A装置中温度/℃ | 室温 | 100 | 500 |
B装置/g | 200.00 | X | 228.00 |
C装置/g | 100.00 | 100.00 | 103.20 |
①表格中 X=______。
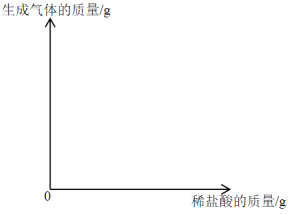
②请你根据表中实验数据,计算出最终生成的 SO3 质量______?(写出计算过程)
(3)加热前后及过程中均需通入 N2,停止加热后继续通 N2 的目的是防止液体倒吸和______
【题目】实验小组同学为验证氢氧化钠的化学性质,设计了下面三个实验。
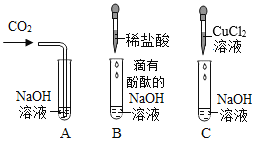
完成实验后,观察到A、B试管均为无色,C试管上层为无色溶液,试管底部有蓝色沉淀生成,C试管中反应的化学方程式是__:将A、B试管和C试管中的上层清液一起倒进一个洁净的烧杯中,观察到烧杯内溶液变为红色。
[提出问题]混合后烧杯内溶液中除酚酞外,含有的溶质是什么?
[查阅资料]碳酸钠溶液显碱性,氯化钙、氯化钡溶液显中性。
[猜想假设]猜想一:氯化钠、碳酸钠
猜想二:氯化钠、氢氧化钠
猜想三:氯化钠、碳酸钠和氢氧化钠
猜想四:氯化钠、碳酸钠、氢氧化钠、盐酸
[交流讨论]小组同学和老师交流后认为猜想_____是错误的;老师告诉同学们猜想二也不合理,理由是_____。
[实验验证]大家对剩余的猜想设计了如下实验进行验证:
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量烧杯中的废液于试管中,滴加适量的氢氧化钙溶液 | 有白色沉淀产生,上层溶液为______色 | 猜想三成立 |
方案二 | 取少量烧杯中的废液于试管中,滴加过量的______溶液 | 产生白色沉淀,上层溶液仍为红色 | 猜想三成立 |
[反思交流] 经小组同学交流讨论后, 认为方案一不能验证猜想三成立, 原因是________。
[拓展应用]以上实验中,若要检验氢氧化钠,必须对碳酸钠进行“屏蔽处理”,否则碳酸钠的存在会对氢氧化钠的检验产生干扰,检验有相似性质的物质,要避开共性,从个性着手,若要检验氯化钠溶液中是否混有盐酸可选用________溶液。