题目内容
在反应:2A+B═C+2D中,A、B、C质量比为5:2:3,若15克A与 足量B反应,可生成D 克,若已知C的相对分子质量为M,则D的相对分子质量是 .在反应X+2Y═R+2M中,已知R和M的相对分子质量比为22:9,当1.6X与Y完全反应后,生成 4.4克R,则在反应中Y和M的质量比 .
考点:质量守恒定律及其应用,根据化学反应方程式的计算
专题:化学用语和质量守恒定律
分析:根据质量守恒定律考虑本题:参加反应的A和B的质量和等于生成的C和D的质量,A、B、C三种物质的质量比为5:2:3,所以生成D的质量为4进行解答.
根据化学方程式和已知条件“R和M的相对分子质量之比为22:9”以及R的质量,列出比例式,即可求出M的质量;根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.则生成的Y的质量=R的质量+M的质量-X的质量;然后写出两者的比,据此选择即可.
根据化学方程式和已知条件“R和M的相对分子质量之比为22:9”以及R的质量,列出比例式,即可求出M的质量;根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.则生成的Y的质量=R的质量+M的质量-X的质量;然后写出两者的比,据此选择即可.
解答:解:在2A+B═C+2D中,A、B、C三种物质的质量比为5:2:3,所以生成D的质量为4,所以A和B质量比为5:2,所以15gA与足量B反应生成12g的D,C和D的质量为3:4,设D的相对分子质量为x,则
2A+B═C+2D
M 2x
3 4
=
,解得x=
,
根据已知条件“R和M的相对分子质量之比为22:9”,则R:2M=22:2×9=22:18,
设生成的M的质量为a,∴22:18=4.4g:a,解得:a=3.6g;
根据质量守恒定律可得Y的质量=4.4g+3.6g-1.6g=6.4g;
∴此反应中Y和M的质量比是6.4g:3.6g=16:9.
故答案为:12;
;16:9.
2A+B═C+2D
M 2x
3 4
| M |
| 2x |
| 3 |
| 4 |
| 2M |
| 3 |
根据已知条件“R和M的相对分子质量之比为22:9”,则R:2M=22:2×9=22:18,
设生成的M的质量为a,∴22:18=4.4g:a,解得:a=3.6g;
根据质量守恒定律可得Y的质量=4.4g+3.6g-1.6g=6.4g;
∴此反应中Y和M的质量比是6.4g:3.6g=16:9.
故答案为:12;
| 2M |
| 3 |
点评:计算相对分子质量时与前面的系数有关,相对分子质量比等于质量比进行列等式.

练习册系列答案
相关题目
在溶液中有FeSO4和CuSO4,加入锌粉后,振荡下列说法不正确的是( )
| A、若有锌粉剩余,且溶液里尚有Cu2+,则必定有Fe2+ |
| B、若有锌粉剩余,则溶液中只有Fe2+ |
| C、若有锌粉剩余,则溶液中只有Zn2+ |
| D、若锌粉无剩余,且溶液中无Cu2+,则一定有Zn2+,但有无Fe2+不能肯定 |
碳的以下用途是利用碳的化学性质在常温下稳定性的是( )
| A、木炭冶金工业上可以炼铁 |
| B、钻石恒久远,一颗永流传 |
| C、石墨做铅笔芯 |
| D、木头做的电线杆埋入地下部分微烧焦 |
某同学将镁和金属X的混合物共2.4g加入足量的稀硫酸,充分反应后得到0.22g H2,则金属X可能是( )
| A、A1 | B、Zn | C、Fe | D、Cu |
下列说法正确的是( )
| A、原子、分子、离子都可以直接构成物质 |
| B、一种元素在同一种化合物中表现出来的化合价相同 |
| C、有单质和化合物生成的反应一定是置换反应 |
| D、根据质量守恒定律,6 g碳在10 g氧气中充分燃烧能生成16 g二氧化碳 |
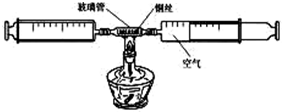 学课外活动小组的同学在查阅资料后知道:铜丝+氧气
学课外活动小组的同学在查阅资料后知道:铜丝+氧气