题目内容
某同学将镁和金属X的混合物共2.4g加入足量的稀硫酸,充分反应后得到0.22g H2,则金属X可能是( )
| A、A1 | B、Zn | C、Fe | D、Cu |
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:假设该金属全部是镁计算出产生氢气质量为0.2g,因为实际产生氢气0.22g,所以另一种金属与镁相比,相同质量时必需产生氢气比锌多.
解答:解:设该金属全部是镁,2.4g镁与硫酸反应产生氢气的质量为y,则:
Mg+H2SO4═MgSO4+H2↑
24 2
2.4g y
根据:
=
,则解得y=0.2g,因为收集到0.22gH2,所以另一种金属产生氢气的质量必须比同质量的镁产生氢气质量多,铝产生的氢气比相同质量的镁产生氢气多,铁、锌产生的氢气比相同质量的镁产生氢气少,所以可能是铝.
故选:A.
Mg+H2SO4═MgSO4+H2↑
24 2
2.4g y
根据:
| 24 |
| 2 |
| 2.4g |
| y |
故选:A.
点评:解答本题关键是要知道假设该金属全部是镁,计算出产生氢气的质量,再与实际产生氢气比较,再进一步分析即可.

练习册系列答案
相关题目
首先提出“空气是由氮气和氧气组成”的科学家是( )
| A、瑞典的舍勒 |
| B、法国的拉瓦锡 |
| C、中国的祖冲之 |
| D、英国的普利斯特里 |
据《扬子晚报》报道,今年4月,陕西汉中市区,一辆运输浓盐酸的车辆发生事故,导致酸液泄漏闹市,经喷水和撒石灰处理后,排除了险情.对喷水和撒石灰做法的叙述错误的是( )
| A、喷水可以减少浓盐酸挥发 |
| B、喷水可以降低盐酸酸性 |
| C、撒石灰为了消除盐酸污染 |
| D、喷水是尽快把盐酸冲进下水道 |
下列关于铁的叙述正确的是( )
| A、铁在潮湿的空气中易生锈 |
| B、铁与稀硫酸反应,生成Fe2(SO4)3和H2 |
| C、能用铁桶盛农药波尔多液 |
| D、铁丝在氧气中剧烈燃烧,火星四射,生成氧化铁 |
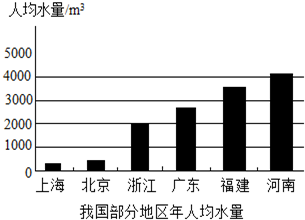 下列是我国部分地区人均水量图和水资源紧缺指标表:
下列是我国部分地区人均水量图和水资源紧缺指标表: