题目内容
15.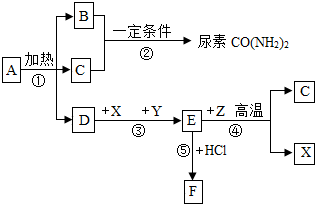 如图表示某些物质间转化关系.A为不含金属元素的盐,可作化肥,X是常见金属,B、C、Y、Z为气体,且B有刺激性气味,F为棕黄色溶液.
如图表示某些物质间转化关系.A为不含金属元素的盐,可作化肥,X是常见金属,B、C、Y、Z为气体,且B有刺激性气味,F为棕黄色溶液.(1)A的化学式为NH4HCO3.
(2)生活中普遍存在着转化③,为防止 ③的发生,可采取的一种措施是涂漆;工业生产中常利用反
应④来炼铁.
(3)反应①提醒我们,在农业生产中保存此化肥的方法是阴凉处保存.
(4)反应⑤的化学方程式为2Fe2O3+6HCl=2FeCl3+3H2O.
(5)反应②的化学方程式为2NH3+CO2$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
分析 根据A为不含金属元素的盐,可作化肥,X是常见金属,B、C、Y、Z为气体,且B有刺激性气味,所以B是氨气,E和盐酸反应回生成棕黄色溶液F,所以F是氯化铁,E是氧化铁,D、X、Y会生成氧化铁,所以D是水,X是铁,Y是氧气,氧化铁和一氧化碳高温生成铁和二氧化碳,所以C是二氧化碳,A是碳酸氢铵,然后将推出的物质进行验证即可.
解答 解:(1)A为不含金属元素的盐,可作化肥,X是常见金属,B、C、Y、Z为气体,且B有刺激性气味,所以B是氨气,E和盐酸反应回生成棕黄色溶液F,所以F是氯化铁,E是氧化铁,D、X、Y会生成氧化铁,所以D是水,X是铁,Y是氧气,氧化铁和一氧化碳高温生成铁和二氧化碳,所以C是二氧化碳,A是碳酸氢铵,经过验证,推导正确,所以A是NH4HCO3;
(2)生活中普遍存在着转化③,为防止 ③的发生,可采取的一种措施是涂漆;工业生产中常利用反应④来炼铁;
(3)反应①提醒我们,在农业生产中保存此化肥的方法是阴凉处保存;
(4)反应⑤是氧化铁和盐酸反应生成氯化铁和水,化学方程式为:2Fe2O3+6HCl=2FeCl3+3H2O;
(5)反应②是氨气和二氧化碳在一定条件下反应生成尿素和水,化学方程式为:2NH3+CO2$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
故答案为:(1)NH4HCO3;
(2)涂漆等,炼铁;
(3)阴凉处保存;
(4)2Fe2O3+6HCl=2FeCl3+3H2O;
(5)2NH3+CO2$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 运用氯化钠和硝酸钾的溶解度表与溶解度曲线回答下列问题:
运用氯化钠和硝酸钾的溶解度表与溶解度曲线回答下列问题:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
(2)曲线上交点的意义是t℃时,两者的溶解度相等
(3)50℃时50g水中加入60g硝酸钾,所得溶液的质量是92.75g.
| A. |  转炉炼钢 | B. |  烟花绽放 | C. |  七彩电灯光 | D. |  烧制陶瓷 |
| A. | 垃圾分类回收、利用 | B. | 汽车使用催化净化装置 | ||
| C. | 大量使用一次性塑料袋 | D. | 开发利用新型能源 |



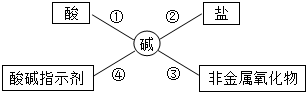 酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题:
酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题: