题目内容
8.氯化钠是日常生活中的必需品,某氯化钠样品中除含氯化钠外,还含有少量的CaCl2和MgCl2以及不溶性杂质.以下是提纯该样品的操作流程图.回答问题: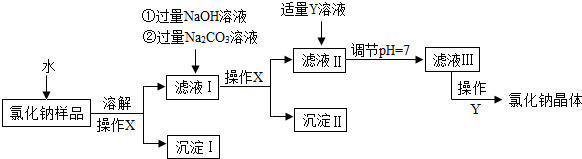
(1)操作X的名称是过滤,玻璃仪器除了玻璃棒,烧杯之外还有漏斗
(2)产生沉淀Ⅱ的化学方程式CaCl2+Na2CO3=2NaCl+CaCO3↓(任写一个)
(3)Y溶液中溶质的化学式是HCl
(4)操作Y是蒸发,玻璃棒的作用是搅拌,防止局部过热,造成液滴飞溅.
分析 根据镁离子用氢氧根离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析.
解答 解:因为镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀;钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,故除掉少量的CaCl2和MgCl2以及不溶性杂质,根据流程图,可知:
(1)操作X,分离可溶物和不溶物,此名称是过滤,过滤操作中用到的玻璃仪器有:烧杯、漏斗、玻璃棒;
(2)氢氧化钠和氯化镁会生成氢氧化镁沉淀、碳酸钠和氯化钙会生成碳酸钙沉淀,所以产生沉淀Ⅱ的化学方程式是:CaCl2+Na2CO3=2NaCl+CaCO3↓;
(3)滤液Ⅱ中含有氯化钠、氢氧化钠、碳酸钠,则为了除掉氢氧化钠、碳酸钠,需要加入的Y溶液为稀盐酸,故其中溶质的化学式是HCl;
(4)操作Y是蒸发,玻璃棒的作用是搅拌,防止局部过热,造成液滴飞溅.
故答案为:(1)过滤,漏斗;
(2)CaCl2+Na2CO3=2NaCl+CaCO3↓;
(3)HCl;
(4)蒸发,搅拌,防止局部过热,造成液滴飞溅.
点评 本题主要考查选择试剂、化学方程式的写法及蒸发操作,完成此题,可以依据物质的性质进行.

练习册系列答案
相关题目
18.下列物质露置在空气中,因发生化学变化而质量变大的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 烧碱 | D. | 氯化钠 |
16.比较类推是学习中常用的思维方法,下列类推正确的是( )
| A. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 化学反应前后元素种类不变,所以燃烧生成二氧化碳的物质中一定含有碳元素 | |
| C. | 单质中一定含一种元素,所以含一种元素的物质一定是单质 | |
| D. | 物质燃烧需要氧气,所以只要有氧气存在物质就能燃烧 |
13.下列除杂设计(括号内为杂质)所选用试剂和操作都正确的是( )
| 序号 | 物 质 | 选用试剂 | 操作 |
| A | CO2(CO) | O2 | 点燃 |
| B | Na OH溶液(Na2CO3) | 稀盐酸 | 加入试剂至不再产生气泡 |
| C | CaCl2溶液(HCl) | CaCO3粉末 | 加入过量的试剂,过滤 |
| D | H2SO4溶液(HCl) | AgNO3溶液 | 加入适量的试剂,过滤 |
| A. | A | B. | B | C. | C | D. | D |
20.现有一种晶体(Na2CO3•nH2O),在不同温度下,可失去部分或全部结晶水,为了测定其组成,在不同温度下加热(温度依次升高),实验结果见下表.坩埚的质量为32.5g,加热前坩埚和晶体的质量为55.7g.求:
(1)第二次加热后坩埚里试样的结晶水的质量分数
(2)计算该晶体中n的值
(1)第二次加热后坩埚里试样的结晶水的质量分数
(2)计算该晶体中n的值
| 实验次序 | 温度 | 冷却后质量(坩埚和样品)/g |
| 1 | T1 | 48.5 |
| 2 | T2 | 44.9 |
| 3 | T3 | 43.1 |
| 4 | T4 | 43.1 |