题目内容
将7.9g的KMnO4加热分解,能得到标准状况下的氧气多少升?(标准状况下氧气的密度是1.429g/L)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据高锰酸钾的质量计算出生成氧气的质量,再除以氧气的密度计算出体积.
解答:解:设生成氧气的质量为x.
2KMnO4
K2MnO4+MnO2+O2↑
316 32
7.9g x
根据:
=
,
解得 x=0.8 g
标准状况下氧气的体积为:
≈0.6 L
答:标准状况下氧气的体积为0.6L.
2KMnO4
| ||
316 32
7.9g x
根据:
| 316 |
| 7.9g |
| 32 |
| x |
解得 x=0.8 g
标准状况下氧气的体积为:
| 0.8g |
| 1.43g/L |
答:标准状况下氧气的体积为0.6L.
点评:带入方程式计算的数据必须是质量,再计算体积时必须先计算出质量,再除以其密度.

练习册系列答案
相关题目
铁是生产和生活中使用最多的金属材料,下列关于铁的叙述错误的是( )
| A、铁生锈时生成四氧化三铁 |
| B、表面涂漆以防止铁生锈 |
| C、铁制品应放置于干燥的环境中 |
| D、保持铁器表面洁净有利于防止铁生锈 |
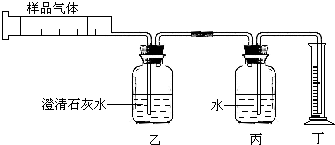 某课外活动小组,欲测定一待旅游开发的溶洞空气中二氧化碳的体积分数,进行如下实验:
某课外活动小组,欲测定一待旅游开发的溶洞空气中二氧化碳的体积分数,进行如下实验: