题目内容
(1)金属原子,最外层电子一般______4,较易______电子;
(2)非金属原子,最外层电子一般______4,较易______电子;
(3)稀有气体原子,最外层电子为______,(He为______),达到稳定.
(2)非金属原子,最外层电子一般______4,较易______电子;
(3)稀有气体原子,最外层电子为______,(He为______),达到稳定.
(1)金属原子的最外层电子数一般少于4个,在反应中容易失去电子而满足最外层8电子的稳定结构,故答案为:少于;失去;
(2)非金属原子的最外层电子数一般多于4个,在反应中容易得到电子而满足最外层8电子的稳定结构,故答案为:多于;得到;
(3)稀有气体的性质稳定,是因其原子的最外层电子数为8(He为2),故答案为:8;2.
(2)非金属原子的最外层电子数一般多于4个,在反应中容易得到电子而满足最外层8电子的稳定结构,故答案为:多于;得到;
(3)稀有气体的性质稳定,是因其原子的最外层电子数为8(He为2),故答案为:8;2.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


 它在表中位置是
它在表中位置是

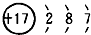 ,该元素在化学反应中容易
,该元素在化学反应中容易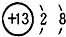 ,该离子带
,该离子带