题目内容
1.化学兴趣小组的同学设计了利用三通管进行如下实验来验证二氧化碳气体的相关性质,实验步骤如下:(整套装置的气密性良好,如图2).
注:整个实验中不考虑反应过程中水分和HCl气体挥发的影响,且图2中产生的气流较缓慢.
步骤Ⅰ.用20mL 的注射器先抽取10mL CO2,再抽取10mL水(如图1),封闭针管后用力振荡,观察到活塞最后停在12mL刻度处.说明在室温下10mL水约能溶解8mL CO2.
步骤Ⅱ.如图2,三通管横放,打开仪器a(填写仪器a名称:分液漏斗)的活塞,观察三通管内产生的实验现象是A处试纸变红,B试纸不变色.
步骤Ⅲ.取图2中的三通管,把贴有试纸A的那端放在酒精灯火焰上加热(如图3),发生的化学反应方程式是H2CO3=H2O+CO2↑.
步骤Ⅳ.将二氧化碳的发生装置与图4相连接,三通管上、下火焰有何变化:下面的蜡烛先熄灭,上面的蜡烛后熄灭;
此实验说明二氧化碳具有不燃烧不支持燃烧、密度比空气大性质.
分析 步骤Ⅰ根据二氧化碳能溶于水分析;
步骤Ⅱ根据二氧化碳能与水化合生成了碳酸分析;
步骤Ⅲ根据碳酸不稳定易分解分析回答;
步骤Ⅳ根据实验的现象分析二氧化碳的性质.
解答 解:步骤Ⅰ.二氧化碳能溶于水,在室温下10mL水约能溶解二氧化碳的体积是:20mL-12mL=8mL;
步骤Ⅱ.如图2,三通管横放,打开仪器a(填写仪器a名称:分液漏斗)的活塞,由于稀盐酸与石灰石反应生成了二氧化碳,二氧化碳能与水化合生成了碳酸,所以观察三通管内产生的实验现象是:A处试纸变红,B试纸不变色.
步骤Ⅲ.取图2中的三通管,把贴有试纸A的那端放在酒精灯火焰上加热,由于碳酸不稳定易分解,发生的化学反应方程式是H2CO3=H2O+CO2↑.
步骤Ⅳ.将二氧化碳的发生装置与图4相连接,三通管上、下火焰的变化是:下面的蜡烛先熄灭,上面的蜡烛后熄灭;此实验说明二氧化碳具有不燃烧不支持燃烧、密度比空气大的性质.
故答为:步骤Ⅰ.8;步骤Ⅱ.分液漏斗,A处试纸变红,B试纸不变色.步骤Ⅲ.H2CO3=H2O+CO2↑.
步骤Ⅳ.下面的蜡烛先熄灭,上面的蜡烛后熄灭;不燃烧不支持燃烧、密度比空气大的性质.
点评 本题通过设计实验考查了二氧化碳的重要性质,实验较新颖,同学们要透过现象看到本质,此题难度中等.

练习册系列答案
相关题目
12.下列物质中,前者是氧化物,后者是化合物的是( )
| A. | 空气、氧气 | B. | 二氧化硫、高锰酸钾 | ||
| C. | 铁、氢气 | D. | 碳、水 |
9.下列实验方案正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去硫酸镁溶液中的硫酸 | 加入过量的Ba(OH)2溶液,过滤 |
| B | 分离氯化钠和硝酸钠固体混合物 | 加水溶解后,过滤,蒸发结晶 |
| C | 鉴别氯化铵和氯化钙 | 分别加入熟石灰,研磨,闻气味 |
| D | 鉴别羊毛织物和涤纶织物, | 分别灼烧,闻气味 |
| A. | A | B. | B | C. | C | D. | D |
13.下列归类错误的是( )
| 选项 | 归类 | 物质(或元素) |
| A | 可燃性气体 | 氢气、一氧化碳、甲烷 |
| B | 三大强酸 | 盐酸 硫酸 碳酸 |
| C | 放热的化学反应 | 中和反应、生石灰与水反应、燃烧 |
| D | 人体中常见微量元素 | 碘、锌、硒、铜等 |
| A. | A | B. | B | C. | C | D. | D |
11.下列关于CO2的用途只利用其物理性质的是( )
| A. | 干冰用于人工降雨 | |
| B. | CO2能用来生产汽水等碳酸饮料 | |
| C. | CO2参加植物的光合作用可提高农作物产量 | |
| D. | CO2用作灭火 |
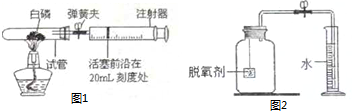 我校化学兴趣小组测定空气中氧气的含量,并改进教材方案.
我校化学兴趣小组测定空气中氧气的含量,并改进教材方案.
