题目内容
11.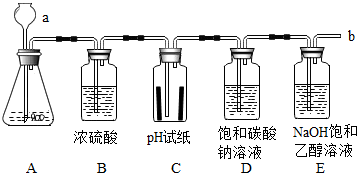 某学习小组用下列装置进行CO2的制取及性质探究实验.
某学习小组用下列装置进行CO2的制取及性质探究实验.资料卡片:20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g.20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g.请根据如图回答下列问题:
(1)图中装置A是用大理石制CO2的装置,仪器a的名称是长颈漏斗;装置A中发生反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,在b处检验是否有CO2逸出的操作是将燃着的木条放在导气管口.
(2)装置C中放有干和湿的pH试纸各一张,当通入CO2一段时间后,湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,实验结论是二氧化碳与水反应生成碳酸,碳酸显酸性.
(3)当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,则反应的化学方程式是CO2+H2O+Na2CO3═2NaHCO3
(4)当通入CO2一段时间后,装置E中观察到的实验现象是出现白色沉淀,则发生反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
分析 (1)认识常见仪器的名称,根据实验室中制取二氧化碳的原理以及二氧化碳的性质来分析;
(2)根据二氧化碳能与水反应生成碳酸,碳酸显酸性来分析;
(3)根据题意,将CO2通入Na2CO3溶液中,只生成NaHCO3,写出反应的化学方程式即可;
(4)根据题干信息,碳酸钠在乙醇中几乎不溶解来分析.
解答 解:(1)仪器a是长颈漏斗,大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳不燃烧也不支持燃烧,所以在b处检验是否有CO2逸出的操作为将燃着的木条放在导管口,观察木条是否熄灭;故填:长颈漏斗;CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在导气管口;
(2)湿的pH试纸上有水,二氧化碳和水反应生成碳酸,碳酸显酸性,故pH约为6,而干燥的pH试纸上没有,二氧化碳不能使之变色;故填:二氧化碳与水反应生成碳酸,碳酸显酸性;
(3)将CO2通入Na2CO3溶液中,只生成NaHCO3,反应的化学方程式为:CO2+H2O+Na2CO3═2NaHCO3.故答案为:CO2+H2O+Na2CO3═2NaHCO3;
(4)氢氧化钠与二氧化碳反应生成碳酸钠和水,而碳酸钠在乙醇是不溶解的,所以看到出现白色沉淀,故填:出现白色沉淀;2NaOH+CO2=Na2CO3+H2O.
点评 本题考查了仪器的名称、二氧化碳的实验室制取方法、二氧化碳的性质以及化学方程式的书写,难度不大.

练习册系列答案
相关题目
1.科学实验中、准确地分析实验数据是得到科学结论的保证.下列4个图象,能正确反映对应关系的是( )
| A. |  常温下,稀释KOH溶液 | |
| B. |  甲烷和过量的氧气在密闭容器中完全反应 | |
| C. | 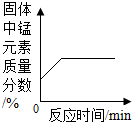 加热一定质量高锰酸钾固体 | |
| D. |  在装有稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量 |
2.下列实验操作中,正确的是( )
| A. | 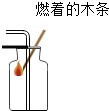 检验CO2是否集满 | B. | 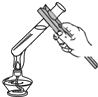 加热液体 | ||
| C. | 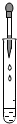 滴加液体 | D. | 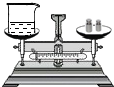 称量NaOH固体质量 |
19. 探究影响化学反应速率的因素
探究影响化学反应速率的因素
(1)发现和提出问题
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是反应物本身的性质.
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是氧气的浓度;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率,温度如何影响反应速率呢?
(2)猜想与假设
温度越高,反应速率越快
(3)收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数.不同温度的稀硫酸(20℃、40℃)
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支.利用上述仪器和药品,补充完成下表的实验报告.
该实验可以观察或测量的量有多种,除了上述观测点外,可以观察或测量的量还有(写一条)相同时间内收集气体的体积(或反应结束所需的时间或消耗等量的锌粒所需的时间或消耗等量的稀硫酸所需的时间)等.
(4)结论与解释
从微观的角度分析“温度越高,反应速率越快”的原因是温度升高,粒子的运动的速率加快,有效碰撞机会增加.
(5)拓展分析
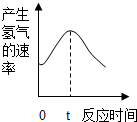
根据其他测定方位,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图所示,请据图分析:时间0-t内,反应速率逐渐加快的主要原因是锌与稀硫酸反应放热,温度升高,反应速率加快,时间t以后,反应速率逐渐减慢的主要原因是随着反应的进行,反应物的浓度越来越小,反应速率减慢.
 探究影响化学反应速率的因素
探究影响化学反应速率的因素(1)发现和提出问题
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是反应物本身的性质.
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是氧气的浓度;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率,温度如何影响反应速率呢?
(2)猜想与假设
温度越高,反应速率越快
(3)收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数.不同温度的稀硫酸(20℃、40℃)
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支.利用上述仪器和药品,补充完成下表的实验报告.
| 观察或测量的量 | 选用的仪器 | 实验步骤 | 实验现象 | 实验结论 |
| 产生相同体积(一试管)的气体所需时间 | 气体发生装置、秒表、胶头滴管、水槽、大试管、 药匙、量筒 | 温度越高,反应速率越快.反应的化学方程式是Zn+H2SO4═ZnSO4+H2↑ |
(4)结论与解释
从微观的角度分析“温度越高,反应速率越快”的原因是温度升高,粒子的运动的速率加快,有效碰撞机会增加.
(5)拓展分析
根据其他测定方位,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图所示,请据图分析:时间0-t内,反应速率逐渐加快的主要原因是锌与稀硫酸反应放热,温度升高,反应速率加快,时间t以后,反应速率逐渐减慢的主要原因是随着反应的进行,反应物的浓度越来越小,反应速率减慢.
6. 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A. | t1℃时甲的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| B. | 乙的溶解度随温度的升高而增大 | |
| C. | 相同温度时,甲的溶解度一定大于乙的溶解度 | |
| D. | 分别将甲、乙的饱和溶液从t2℃降至t1℃时,所得溶液中溶质的质量分数相等 |
16.下列生活生产中的现象不利于我国可持续发展的是( )
| A. | 农村直接焚烧秸秆肥田 | B. | 大力发展电动汽车,实现节能减排 | ||
| C. | 远离烟草、拒绝毒品 | D. | 改进燃煤炉灶,促进燃料充分燃烧 |
20.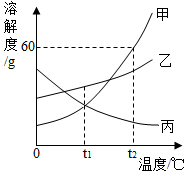 图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
 图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )| A. | t1℃时,三种固体物质的溶解度关系为乙>甲=丙 | |
| B. | t2℃100g甲物质饱和溶液中含有60g甲 | |
| C. | 将丙物质饱和溶液变为不饱和溶液,可采用升温的方法 | |
| D. | t2℃时,分别用100g水配制甲、乙的饱和溶液,再降温到t1℃,析出无水晶体的质量:甲>乙 |
11.天天同学将打磨后的铜片小心的滑入装有稀硫酸的试管中并仔细观察,他一直没有看到明显的现象发生,于是他想到要给试管进行加热试一试,当加热沸腾一段时间以后,溶液开始变为蓝色,同时还观察到持续有较多的气泡产生,
【提出问题】生成的是什么呢?
【大胆猜想】你的猜测依据是质量守恒定律.
(1)可能是氢气;(2)可能是氧气;(3)可能是二氧化硫.
【查阅资料】:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑
【实验方案】
【交流与讨论】铜与稀硫酸加热一段时间后能发生反应,针对这一现象的上述猜想与验证,你认为下列解释合理的是(6).
(4)温度升高增强了金属铜的活动性
(5)升高温度加快了该化学反应速率
(6)加热使水分蒸发后变成了浓硫酸
【拓展思维】通过上述研究,你获得的新思考是:铜可以和浓硫酸反应.
【提出问题】生成的是什么呢?
【大胆猜想】你的猜测依据是质量守恒定律.
(1)可能是氢气;(2)可能是氧气;(3)可能是二氧化硫.
【查阅资料】:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 |
| 收集满一试管的纯净气体,用燃着的木条伸入试管内 | 气体没有燃烧,木条熄灭 | 猜想(1)(2)不成立 |
| 将气体通入装有澄清石灰水的试管中 | 澄清石灰水变浑浊 | 猜想(3)成立,其反应方程式为SO2+Ca(OH)2=CaSO3↓+H2O |
(4)温度升高增强了金属铜的活动性
(5)升高温度加快了该化学反应速率
(6)加热使水分蒸发后变成了浓硫酸
【拓展思维】通过上述研究,你获得的新思考是:铜可以和浓硫酸反应.
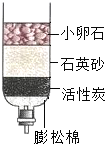 水是人们生活生产中应用最多的物质:
水是人们生活生产中应用最多的物质: