题目内容
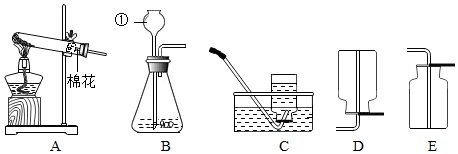
5.根据如图所示的实验回答问题.
(1)指出甲实验的不足之处瓶内未预先加入适量水,或瓶内未预先加入适量氢氧化钠溶液.
(2)已知氯化铁溶液、硫酸铜溶液均可做过氧化氢制氧气的催化剂.乙实验的目的是比较相同量、相同浓度的氯化铁溶液和硫酸铜溶液对过氧化氢分解的催化效果;
请写出乙实验中反应的化学方程式2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(3)丙实验①、②是粗盐提纯实验中的两步,做完步骤①后,滤液仍然浑浊,其原因可能是滤纸破损,液面高于滤纸边缘等;步骤②中,当观察到出现较多固体时,停止加热.
分析 (1)硫在氧气中燃烧生成二氧化硫,二氧化硫有毒,扩散到空气中污染环境;
(2)通过对比试验可以比较氯化铁溶液和硫酸铜溶液的催化效果;
过氧化氢在催化剂作用下分解生成水和氧气;
(3)过滤后,滤液仍然浑浊,其原因可能是滤纸破损,液面高于滤纸边缘等;
步骤②中,当观察到出现较多固体时,停止加热.
解答 解:(1)甲实验的不足之处是:瓶内未预先加入适量水,或瓶内未预先加入适量氢氧化钠溶液来吸收二氧化硫.
故填:瓶内未预先加入适量水,或瓶内未预先加入适量氢氧化钠溶液.
(2)乙实验的目的是比较相同量、相同浓度的氯化铁溶液和硫酸铜溶液对过氧化氢分解的催化效果;
乙实验中过氧化氢在催化剂作用下分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
故填:比较相同量、相同浓度的氯化铁溶液和硫酸铜溶液对过氧化氢分解的催化效果; 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(3)做完步骤①后,滤液仍然浑浊,其原因可能是滤纸破损,液面高于滤纸边缘等;
步骤②中,当观察到出现较多固体时,停止加热.
故填:滤纸破损,液面高于滤纸边缘等;出现较多固体.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
16.现有A、B、C三种金属,已知A能将C从它的溶液中置换出来,B能与盐酸或稀硫酸反应产生氢气,A不能与盐酸或稀硫酸反应.则这三种金属活动性由强到弱的顺序是( )
| A. | B>A>C | B. | B>C>A | C. | A>B>C | D. | 无法判断 |
13.发展绿色食品,避免“白色污染”,增强环保意识,是保护环境,提高人类生存质量的主要措施.通常的“白色污染”是指( )
| A. | 冶炼厂排放的白色烟尘 | B. | 石灰窑放出的白色粉尘 | ||
| C. | 聚乙烯等白色塑料垃圾 | D. | 白色建筑材料垃圾 |
20.类推是学习中常用的思维方法.现有一下类推结果,其中错误的是
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④复分解反应的反应物为两种化合物,生成物也是两种化合物,所以反应物为两种化合物,生成物也是两种化
合物的反应一定是复分解反应.( )
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④复分解反应的反应物为两种化合物,生成物也是两种化合物,所以反应物为两种化合物,生成物也是两种化
合物的反应一定是复分解反应.( )
| A. | 只有 ① | B. | 只有 ①②③ | C. | 只有②③④ | D. | ①②③④ |

 小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )