题目内容
10.下列属于纯净物的是( )| A. | 冰水混和物 | B. | 液化后的空气 | ||
| C. | “蒙牛”纯牛奶 | D. | 含有两种分子的气体 |
分析 本题考查利用纯净物的概念来判断物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子
解答 解:A、冰水混合物是由水一种物质组成,属于纯净物,故A正确;
B、液化后的空气中含有氧气、氮气、二氧化碳等物质,属于混合物,故B错;
C、“蒙牛”纯牛奶中含有蛋白质、油脂等物质,属于混合物,故C错;
D、含有两种分子的气体中含有两种物质,属于混合物,故D错.
故选A.
点评 在熟悉概念的基础上能从宏观和微观两个方面来判断纯净物和混合物,还要从社会实践中了解生活中常见物质的组成.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.四氧化三铁可用于医疗器械、电子等工业.某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液.
(3)制备Fe3O4的实验流程如图:
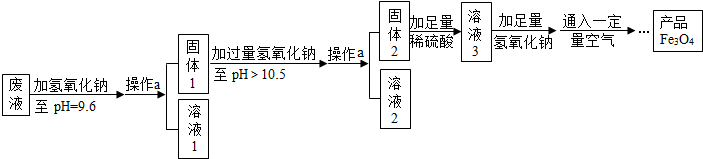
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为(写一个即可)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4【或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4】.
(2)溶液1所含溶质有(至少写两种)硫酸镁、硫酸钠;溶液3所含溶质的主要成分为硫酸亚铁.
(3)该实验取废液100g,最终得到产品四氧化三铁质量为2.32g,则原废液中硫酸亚铁溶质的质量分数不低于4.56%(精确到0.01%).
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为(写一个即可)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4【或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4】.
(2)溶液1所含溶质有(至少写两种)硫酸镁、硫酸钠;溶液3所含溶质的主要成分为硫酸亚铁.
(3)该实验取废液100g,最终得到产品四氧化三铁质量为2.32g,则原废液中硫酸亚铁溶质的质量分数不低于4.56%(精确到0.01%).
15. 57、用下图装置测定因存放不当而部分变成碳酸钠的烧碱中氢氧化钠的质量分数.所取样本8.00g,锥形瓶质量为140.00g,加入足量的稀硫酸(质量为50.00g),每隔相同时间就读数一次,数据如下表:
57、用下图装置测定因存放不当而部分变成碳酸钠的烧碱中氢氧化钠的质量分数.所取样本8.00g,锥形瓶质量为140.00g,加入足量的稀硫酸(质量为50.00g),每隔相同时间就读数一次,数据如下表:
①Na2CO3中钠元素与碳元素、氧元素的质量比是23:6:24;
②计算样品中氢氧化钠的质量分数;
③假设实验中硫酸恰好完全反应,那么该稀硫酸中硫酸的质量分数?
 57、用下图装置测定因存放不当而部分变成碳酸钠的烧碱中氢氧化钠的质量分数.所取样本8.00g,锥形瓶质量为140.00g,加入足量的稀硫酸(质量为50.00g),每隔相同时间就读数一次,数据如下表:
57、用下图装置测定因存放不当而部分变成碳酸钠的烧碱中氢氧化钠的质量分数.所取样本8.00g,锥形瓶质量为140.00g,加入足量的稀硫酸(质量为50.00g),每隔相同时间就读数一次,数据如下表:| 读数次数 | 质量/g | |
| 锥形瓶+试样+稀硫酸 | 1 | 197.64 |
| 2 | 197.48 | |
| 3 | 197.26 | |
| 4 | 197.16 | |
| 5 | 197.12 | |
| 6 | 197.12 |
②计算样品中氢氧化钠的质量分数;
③假设实验中硫酸恰好完全反应,那么该稀硫酸中硫酸的质量分数?
2.下列实验设计正确的是( )
| A. | 用托盘天平称取5.62g蔗糖 | B. | 用浓硫酸干燥NH3 | ||
| C. | 用KMnO4溶液区分SO2和CO2 | D. | 用活性炭使硬水转化为软水 |

