题目内容
18.我国首台使用二甲醚为燃料的城市客车有效地解决了公交车冒黑烟的问题.已知二甲醚的化学式为C2H6O,二甲醚的相对分子质量是46,其中碳、氢元素的质量比为4:1.分析 根据相对分子的质量为组成分子的各原子的相对原子质量之和,化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答.
解答 解:根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得二甲醚的相对分子质量为12×2+6+16=46;
根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得二甲醚中碳元素与氢元素的质量比为(12×2):6=4:1.
故答案为:46;4:1.
点评 解答此类题必须区分清:化合物中各元素质量比与原子个数比,才能顺利解答.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
8.化学反应有不同的分类方法.关于下列反应说法错误的是( )
(1)Mg$→_{点燃}^{O_{2}}$MgO (2)MgO$\stackrel{稀H_{2}SO_{4}}{→}$MgSO4
(3)Mg$\stackrel{稀HCl}{→}$MgCl2 (4)MgCl2$\stackrel{NaOH溶液}{→}$Mg(OH)2.
(1)Mg$→_{点燃}^{O_{2}}$MgO (2)MgO$\stackrel{稀H_{2}SO_{4}}{→}$MgSO4
(3)Mg$\stackrel{稀HCl}{→}$MgCl2 (4)MgCl2$\stackrel{NaOH溶液}{→}$Mg(OH)2.
| A. | (1)属于吸热反应 | B. | (3)属于置换反应 | C. | (3)属于放热反应 | D. | (4)属于复分解反应 |
13.生铁和钢的主要区别在于( )
| A. | 两者是由两类不同元素组成 | B. | 生铁是混合物,钢是纯净物 | ||
| C. | 生铁是合金,钢不是合金 | D. | 生铁含碳量比钢多,故性能有差异 |
10.下列属于纯净物的是( )
| A. | 冰水混和物 | B. | 液化后的空气 | ||
| C. | “蒙牛”纯牛奶 | D. | 含有两种分子的气体 |
7.下列除杂设计(括号内为杂质)正确的是( )
| 序号 | 物 质 | 选用试剂 | 操 作 |
| A | CO2(HCl) | NaOH溶液 | 洗气 |
| B | CaO(CaCO3) | H2O | 加入足量的水,充分溶解,过滤 |
| C | KNO3溶液(K2CO3) | 稀盐酸 | 加入适量的盐酸至不再产生气泡为止 |
| D | NaCl溶液(CaCl2) | ①Na2CO3溶液 ②稀盐酸 | 先加入过量试剂①,过滤;再向滤液中加入适量试剂② |
| A. | A | B. | B | C. | C | D. | D |
3.元素之间的本质区别是( )不同.
| A. | 相对原子质量 | B. | 最外层电子数 | C. | 核外电子数 | D. | 质子数 |
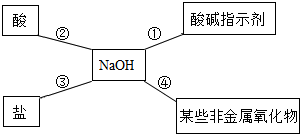 在学习碱的过程中,小红同学用如图总结了NaOH的四条化学性质.
在学习碱的过程中,小红同学用如图总结了NaOH的四条化学性质.