题目内容
14.如图为某化工企业生产流程示意图,有关说法正确的是( )
| A. | ①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X中铁的化合价为+2价 | |
| B. | ③中氩气(Ar)作反应物 | |
| C. | ②中合成的甲醇属于氧化物,且在空气中充分燃烧能生成二氧化碳和水 | |
| D. | ②中为使原料全部转化为甲醇,理论上CO和H2的质量比为7:1 |
分析 A.根据在化合物中正负化合价代数和为零考虑;
B.根据氩气的化学性质来分析;
C.根据氧化物的概念来分析;
D.根据氢气和一氧化碳反应的方程式考虑质量比.
解答 解:A.设FeTiO3中Ti的化合价是x.FeTiO3中Fe的化合价是+2价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则得到方程(+2)+x+(-2)×3=0.解得,x=+4 所以钛酸亚铁(FeTiO3)中钛元素的化合价是+4价,故错误;
B.氩气是一种稀有气体,化学性质稳定,在反应过程中作保护气,不是反应物,故错误;
C.甲醇中含有三种元素,不是氧化物,故错误;
D.根据从化学方程式2H2+CO═CH3OH
4 28
由此可知一氧化碳和氢气的质量比是:28:4=7:1,故正确.
故选D.
点评 本题主要考查了化合价的计算、化学方程式的书写以及质量守恒定律的应用,同时考查了学生从题目中获取信息并运用的能力.计算元素的化合价时一定要注意,一定不要忘记填上正号.

练习册系列答案
相关题目
5.下列各组物质,要借助酸碱指示剂才能判断反应( )
| A. | CaCO3+HCl | B. | Fe2O3+HCl | C. | Fe+H2SO4 | D. | NaOH+H2SO4 |
2.通过下列实验得出的结论中,正确的是( )
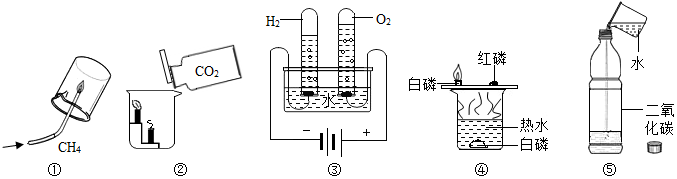
①可说明甲烷是由氢元素和碳元素组成
②可说明二氧化碳的密度比空气大,且二氧化碳不能燃烧也不支持燃烧
③可说明水是由氢元素、氧元素组成
④可说明白磷的着火点比红磷低
⑤可说明二氧化碳具有酸性.

①可说明甲烷是由氢元素和碳元素组成
②可说明二氧化碳的密度比空气大,且二氧化碳不能燃烧也不支持燃烧
③可说明水是由氢元素、氧元素组成
④可说明白磷的着火点比红磷低
⑤可说明二氧化碳具有酸性.
| A. | ①②③④ | B. | ②③④ | C. | ②③④⑤ | D. | ①②③④⑤ |
9.下列四个实验中只需要完成三个就可以证明铁、铜、银三种金属的活动性顺序.其中不必进行的是( )
| A. | 将铁片放入稀盐酸中 | B. | 将铜片放入稀硫酸中 | ||
| C. | 将铁片放入硝酸银溶液中 | D. | 将铜片放入硝酸银溶液中 |
3.下列各方程式中,书写正确是( )
| A. | 2P+5O2═P2O5 | B. | 4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$2 Fe2O3 | ||
| C. | C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | D. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 |
16.某学校在探究铝的化学性质时,实验情况如下:
[提出问题]:铝片放入稀硫酸中,开始时为什么没有明显现象?
[提出假设]:假设1:铝片表面有致密的氧化膜阻碍了反应的进行
假设2:所用稀硫酸的浓度太小
假设3:铝片与稀硫酸反应需要加热
[实验设计]:
你选择的假设是1或2或3.请选择恰当的实验用品进行实验,
证明假设成立.
有以下实验用品:大小相同的铝片、l0%的稀硫酸、30%的稀硫酸、氯化钠、
试管、试管夹、酒精灯、镊子、药匙、砂纸
[评价与反思]:通过这次探究,你从中得到的启示是:善于发现问题,大胆质疑,勇于探究.
| 实验操作 | 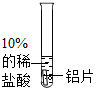 |
| 实验现象 | 开始时.铝片表面没有明显现象 |
[提出假设]:假设1:铝片表面有致密的氧化膜阻碍了反应的进行
假设2:所用稀硫酸的浓度太小
假设3:铝片与稀硫酸反应需要加热
[实验设计]:
你选择的假设是1或2或3.请选择恰当的实验用品进行实验,
证明假设成立.
有以下实验用品:大小相同的铝片、l0%的稀硫酸、30%的稀硫酸、氯化钠、
试管、试管夹、酒精灯、镊子、药匙、砂纸
| 实验步骤(文字叙述或图示可) | 观察到的现象 | 结论 |
| 假设成立 |
 A~H是初中化学中常见的物质,它们都含有同一种元素,F是相对分子质量最小的有机物,B、C组成元素相同,A是一种单质,D是一种含有三种元素的白色不溶于水的固体.
A~H是初中化学中常见的物质,它们都含有同一种元素,F是相对分子质量最小的有机物,B、C组成元素相同,A是一种单质,D是一种含有三种元素的白色不溶于水的固体.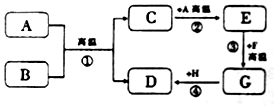 A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示,请回答:
A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示,请回答: