题目内容
15.(1)将源水处理成自来水的过程中需加入生石灰,生石灰与水反应的化学方程式为CaO+H2O═Ca(OH)2.(2)20℃时,氯化钠的溶解度为36g,则20℃时氯化钠饱和溶液中溶质和溶剂的质量比为9:25.
(3)为了进行农业选种,现将200g 30%的氯化钠溶液稀释为10%的氯化钠溶液,需要加水的质量为400.
分析 (1)根据生石灰与水反应生成氢氧化钙解答;
(2)根据溶解度的意义解答;
(3)根据溶液的溶质质量分数可知一定量溶液中所含有溶质的质量,而用浓溶液配制稀溶液时溶质的质量不变,则利用溶质的质量前后相等列等式来解答.
解答 解:
(1)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;
(2)20℃时,氯化钠的溶解度为36g,说明100g水中最多溶解36g氯化钠,则20℃时氯化钠饱和溶液中溶质和溶剂的质量比为36g:100g=9:25;
(3)根据配制前后溶质的质量不变,设需蒸馏水的质量为xg,则
200g×30%═(200+x)g×10%
解得x═400g
答案:
(1)CaO+H2O═Ca(OH)2(2)9:25 (3)400 g
点评 本题考查浓溶液稀释为稀溶液的计算,直接利用“浓溶液质量×浓溶液中溶质的质量质量分数=稀溶液质量×稀溶液中溶质的质量分数”来解答此类习题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列有关实验操作的说法中,错误的是( )
| A. | 做氢气燃烧的实验前要先检验纯度再点燃 | |
| B. | 做一氧化碳还原氧化铜实验时要先通一段时间一氧化碳再加热 | |
| C. | 用PH试纸测溶液的酸碱度时,要先将试纸润湿再滴待测液 | |
| D. | 稀释浓硫酸时要先在烧杯中加水,再加浓硫酸并用玻璃棒不断搅拌 |
6.下列说法正确的是( )
| A. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 | |
| B. | 侯德榜制碱法,制出的火碱又叫烧碱 | |
| C. | 花香四溢,说明分子在不断地运动 | |
| D. | 铝比铁的抗锈蚀性能强,说明铝的金属活动性比铁弱 |
3.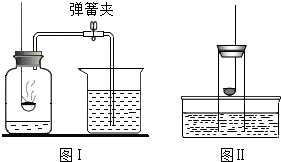 下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )
下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )
 下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )
下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )| A. | 不能用木炭代替红磷 | |
| B. | 图II所示装置也可以测定空气中氧气含量 | |
| C. | 图I中进入集气瓶的水约占烧杯中水的五分之一 | |
| D. | 氮气不与红磷反应且难溶于水,是设计该实验的依据之一 |
10. 糕点疏松剂的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
糕点疏松剂的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
【探究实验一】碳酸氢钠溶液的酸碱性:用pH试纸测得碳酸氢钠溶液的pH约为9,由此得出结论是碳酸氢钠溶液呈碱性.
【探究实验二】碳酸氢钠的热稳定性:取一定量碳酸氢钠放在铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊.
(3)通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
(4)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O..
 糕点疏松剂的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
糕点疏松剂的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.【探究实验一】碳酸氢钠溶液的酸碱性:用pH试纸测得碳酸氢钠溶液的pH约为9,由此得出结论是碳酸氢钠溶液呈碱性.
【探究实验二】碳酸氢钠的热稳定性:取一定量碳酸氢钠放在铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊.
(3)通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 产物含Na2CO3 |
| ② | 取操作①后的上层清液于试管B中,滴加酚酞溶液 | 溶液不变色 | 产物不含NaOH |
7.据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与
小组同学共同完成以下探究:

【提出问题1】固体A中的成分是什么?
【查阅资料】
①CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
②碳酸钾与碳酸钠性质相似,在溶液中都能与氢氧化钙发生复分解反应.
【猜想与假设】甲同学:只有CaCO3 乙同学:CaCO3、Ca(OH)2 丙同学:CaCO3、CaO
甲、乙两位同学认为丙同学的猜想不合理,理由是CaO+H2O=Ca(OH)2(用化学方程式表示).
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了下述实验:
【反思与评价】小组同学讨论后认为,甲同学的实验不能证明他的猜想,理由是CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3;而乙同学的实验能证明他的猜想,因此小组同学确定了固体A的成分.
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】猜想1:KOH、K2CO3 猜想2:KOH、Ca(OH)2 猜想3:KOH
【表达与交流】结合上述实验,同学们讨论确定了猜想2正确,理由是反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2CO3═CaCO3↓+2KOH.
小组同学共同完成以下探究:

【提出问题1】固体A中的成分是什么?
【查阅资料】
①CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
②碳酸钾与碳酸钠性质相似,在溶液中都能与氢氧化钙发生复分解反应.
【猜想与假设】甲同学:只有CaCO3 乙同学:CaCO3、Ca(OH)2 丙同学:CaCO3、CaO
甲、乙两位同学认为丙同学的猜想不合理,理由是CaO+H2O=Ca(OH)2(用化学方程式表示).
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了下述实验:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 自己的猜想正确 |
| 乙同学:取少量固体于试管中,加水溶解后过滤,向滤液中加入酚酞溶液 | 滤液变为红色 | 自己的猜想正确 |
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】猜想1:KOH、K2CO3 猜想2:KOH、Ca(OH)2 猜想3:KOH
【表达与交流】结合上述实验,同学们讨论确定了猜想2正确,理由是反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2CO3═CaCO3↓+2KOH.
4.物质的性质决定了物质的用途.下列几种常见物质的性质、用途不一致的是( )
| A. | 氮气 性质稳定 保护气 | |
| B. | 酒精 可燃性 消毒剂 | |
| C. | 食醋 酸性 除水垢 | |
| D. | 干冰 升华吸热 人工降雨 |
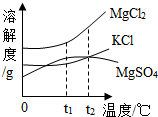 食盐在生产和生活中具有广泛的用途.
食盐在生产和生活中具有广泛的用途.