题目内容
20. 食盐在生产和生活中具有广泛的用途.
食盐在生产和生活中具有广泛的用途.(1)去除粗盐中难溶性的杂质,主要实验步骤有:溶解、过滤、蒸发.在过滤操作中,璃棒的作用是引流.
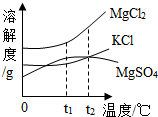
(2)晒盐场经常利用晾晒海水得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图.将t1℃时3种物质的饱和溶液升温到t2℃时,3种溶液溶质的质量分数由小到大的顺序是MgCl2>MgSO4>KCl.
分析 (1)根据在粗盐溶解、过滤、蒸发 过程中,玻璃棒所起作用进行分析;
(2)根据某一温度时物质溶解度的比较方法,溶解度越大,溶质的质量分数越大考虑.
解答 解:(1)在粗盐提纯的步骤是溶解、过滤、蒸发,在过滤操作中,璃棒的作用是引流;
(2)(3)虽然是升温到t2℃,但是由于没有加入溶质,所以对氯化镁和氯化钾质量分数计算依旧要按照t1℃时计算,而硫酸镁温度变化了,溶解度降低了,但是依旧比t1℃的氯化钾的溶解度大,所以从t1℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t1℃时它们的溶解度小到大顺序是KCl溶液、MgSO4溶液、MgCl2溶液;根据饱和溶液溶质的质量分数=$\frac{溶解度}{100g+溶解度}$×100%可知,溶解度越大,饱和溶液溶质的质量分数,故3种溶液溶质的质量分数由小到大的顺序是KCl溶液、MgSO4溶液、MgCl2溶液.
故答案为:
(1)蒸发 引流 (2)MgCl2>MgSO4>KCl
点评 此题考查溶解度知识的具体应用,对学生深入理解溶解度的概念有一定帮助,同时也复习了有关混合物分离的一些常识性的基础知识.

练习册系列答案
相关题目
11.下列说法正确的是( )
| A. | PH=0的溶液显中性,不能使酚酞变色 | |
| B. | 正常雨水的PH为7,酸雨的PH<7 | |
| C. | CO2气体中有水蒸气,可以用氢氧化钠溶液干燥 | |
| D. | 工业废气中的二氧化硫,可以用石水浆吸收处理,防止空气污染 |
5.下图所示的化学实验基本操作中,正确的是( )
| A. |  向试管中加入锌粒 | B. |  过滤 | ||
| C. |  检查装置气密性 | D. |  点燃酒精灯 |




