题目内容
12.虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力.下列有关它的说法正确的是( )| A. | 虾青素是一种氧化物 | |
| B. | 虾青素是由96个原子构成 | |
| C. | 虾青素中碳元素的质量分数为80.5% | |
| D. | 虾青素的相对分子质量是596g |
分析 A.根据氧化物是指由两种元素组成且其中一种是氧元素的化合物进行判断;
B.根据物质的构成来分析;
C.根据根据化合物中元素分数的计算方法来分析;
D.根据相对分子质量的单位考虑.
解答 解:A.根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,由此可判断虾青素不属于氧化物;故错误;
B.虾青素是由虾青素分子构成的,而不是由原子直接构成的,故错误;
C.虾青素中碳元素的质量分数=$\frac{12×40}{12×40+1×52+16×4}×100%$=80.5%,故正确;
D.相对分子质量的单位是1省略不写,故错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列说法正确的是( )
| A. | 相对原子质量约等于质子数与电子数之和 | |
| B. | 同种元素组成的物质一定是单质 | |
| C. | 阳离子的核外电子数小于核内质子数 | |
| D. | 化学变化过程中分子数一定不会改变 |
3.铁制品不能盛放下列哪种药品( )
| A. | 稀HCl | B. | MgSO4溶液 | C. | 氯化钠溶液 | D. | 铁屑 |
20.下列化学方程式书写正确的是( )
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | 2KClO3═2KCl+3O2 | ||
| C. | C+2CuO═2Cu+CO2 | D. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 |
7.蜡烛燃烧生成了二氧化碳和水,根据质量守恒定律得知蜡烛中一定含有的元素是( )
| A. | 碳 | B. | 氢 | C. | 碳、氢、 | D. | 碳、氢、氧 |
17.下列物质不属于溶液的是( )
| A. | 生理盐水 | B. | 消毒酒精 | C. | 液氧 | D. | 食醋 |
2.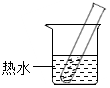 如表是KNO3在不同温度时的溶解度,请回答下列问题.
如表是KNO3在不同温度时的溶解度,请回答下列问题.
(1)20℃时,在装有5g KNO3晶体的试管中,加入10g水并充分振荡,此时所得溶液为饱和(选填“饱和”或“不饱和”)溶液.
(2)将该试管放入盛有热水的烧杯中,使试管内溶液温度升至40℃,此时试管内的溶液中溶剂与溶质的质量比为2:1.
(3)20℃时,不能(填“能”或“不能”)配制溶质质量分数为31.6%的KNO3溶液.
(4)60℃时,100gKNO3饱和溶液,恒温蒸发10g水后,可析出KNO3的质量为11g.
 如表是KNO3在不同温度时的溶解度,请回答下列问题.
如表是KNO3在不同温度时的溶解度,请回答下列问题.| 温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)将该试管放入盛有热水的烧杯中,使试管内溶液温度升至40℃,此时试管内的溶液中溶剂与溶质的质量比为2:1.
(3)20℃时,不能(填“能”或“不能”)配制溶质质量分数为31.6%的KNO3溶液.
(4)60℃时,100gKNO3饱和溶液,恒温蒸发10g水后,可析出KNO3的质量为11g.
 将“宏观物质、微观粒子、化学符号”统一起来是学好化学必有的思维方法.如图是某化学反应的微观示意图,请回答:
将“宏观物质、微观粒子、化学符号”统一起来是学好化学必有的思维方法.如图是某化学反应的微观示意图,请回答: 表示的物质是水;
表示的物质是水;